1、选择题 下列离子方程式正确的是( )
A.钠与水反应:2Na+2H2O═2Na++2OH-+H2↑
B.氧化钠与盐酸反应:O2-+2H+═H2O
C.CaCO3悬浊液中通CO2:C032-+CO2+H2O═2HCO3-
D.小苏打溶液与NaOH溶液混合:HCO3-+OH-═CO32-+H2O
2、填空题 除去下列物质中所混有的少量杂质,指明应加入的试剂,写出有关的离子反应方程式.
(1)Fe粉(Al粉):试剂______?离子方程式______;
(2)FeCl2溶液(FeCl3):试剂______?离子方程式______;
(3)NaHCO3溶液(Na2CO3):试剂______离子方程式______.
3、选择题 下列离子方程式书写正确的是( )
A.铜片插入硝酸银溶液中?Cu+Ag+=Cu2++Ag
B.碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O
C.硫酸铜溶液与氢氧化钡溶液反应:Ba2++s
═BaSO4↓
D.铁与稀硫酸反应:Fe+2H+═Fe2++H2↑
4、填空题 (1)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸铜溶液的反应?
②碳酸钠和足量稀硫酸的反应?
(2)根据下列离子方程式,各写一个符合条件的化学 方程式
方程式
①Fe+2H+====Fe2++H2↑?
②HCO3-+ H+====CO2↑+ H2O??
5、简答题 某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
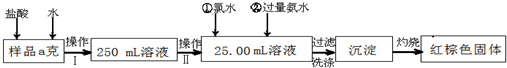
请根据上面流程,回答以下问题:
(1)操作?I?所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有______(填自选仪器名称),操作?II?必须用到的仪器是______?(从以下选项中选择,填编号).
A.50mL烧杯 B.50mL量筒?C.25mL碱式滴定管 D.25mL酸式滴定管
(2)加入试剂①和②后发生反应的离子反应方程式为:______
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是______.
(4)若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:______.
(5)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是:
______?(用化学方程式表示)