1、选择题 下列实验操作正确且能达到目的的是
A.稀释浓硫酸时,将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜以加快反应速率
C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
参考答案:B
本题解析:略
本题难度:简单
2、简答题 氨基磺酸(H2NSO3H)是一元固体强酸,溶于水和液氨,不溶于乙醇.在工业上用作酸性清洗剂、阻燃剂、磺化剂.用尿素[CO(NH2)2]和发烟硫酸(溶有SO3的硫酸)为原料合成氨基磺酸的路线如下:

(1)重结晶用10%~12%的硫酸作溶剂而不用水作溶剂的原因是______.
(2)“磺化”步骤中所发生的反应为:
①CO(NH2)2(s)+SO3(g)?H2NCONHSO3H(s)△H<0
②H2NCONHSO3H+H2SO4?2H2NSO3H+CO2↑
“磺化“过程应控制反应温度75~80℃,若温度高于80℃,氨基磺酸的产率会降低,原因是______.
(3)测定产品中氨基磺酸纯度的方法如下:称取7.920g产品配成l000mL待测液,量取25.00mL待测液于锥形瓶中,加入2mL?0.2mol?L-1稀盐酸,用淀粉碘化钾试剂作指示剂,逐滴加入0.080mol?L-1NaNO2溶液,当溶液恰好变蓝时,消耗NaNO2溶液25.00mL,此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2.
①写出氨基磺酸与NaNO2溶液反应的化学方程式______.
②产品中氨基磺酸的质量分数为______.
(4)以酚酞为指示剂,用NaOH进行酸碱中和滴定也能测定产品中氨基磺酸的纯度,测定结果通常比NaNO2法偏高,原因是氨基磺酸中混有______杂质.
参考答案:(1)反应H2NCONHSO3H+H2SO4?2H2NSO3H+CO2↑是可逆反应,硫酸浓度增大,平衡向正反应方向移动,所以能抑制氨基磺酸的溶解,
故答案为:氨基磺酸在硫酸溶液中的溶解度比在水中的溶解度小;
(2)温度越高,三氧化硫气体逸出速率加快,且CO(NH2)2(s)+SO3(g)?H2NCONHSO3H(s)是放热反应,升高温度,平衡向逆反应方向移动,从而抑制氨基磺酸的产率,
故答案为:温度高,SO3气体逸出加快,使反应①转化率降低.温度高,反应①平衡向逆反应方向移动;
(3)①氨基磺酸与NaNO2溶液反应的化学方程式:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O,故答案为:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O;
②当溶液变蓝色时,说明H2NSO3H恰好完全反应,氨基磺酸和亚硝酸钠的反应方程式为:H2NSO3H+NaNO2=NaHSO4+N2↑+H2O,
根据方程式知,n (H2NSO3H)=n(NaNO2)=25.00×l0-3×0.08000 mol?L-1=2.000×l0-3 mol,
ω(H2NSO3H)=2.000×10-3mol×97g/mol7.920g×25ml1000ml×100%=98.0%,
故答案为:98.0%;
(4)用氢氧化钠测定氨基磺酸的纯度,测定结果通常比NaNO2法偏高,说明还有其它物质和氢氧化钠反应,能和氢氧化钠反应的物质是硫酸,故答案为:硫酸.
本题解析:
本题难度:一般
3、实验题 (9分)用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
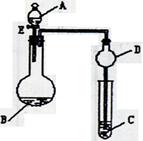
(1)图中D装置在实验中的作用是??。
(2)若 A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式为?。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现象是??;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3(碘酸为强酸),写出该反应的离子反应方程式?。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是?,C中发生反应的离子方程式为?。
参考答案:(9分)⑴防倒吸(1分)
⑵2H2S + O2 ="=" 2S ↓+ 2 H2O? (2分)
⑶有气泡出现,同时溶液由无色变成蓝色(1分);6H2O +I2 +5Cl2===2IO3- + 10Cl- +12H+? (2分)
⑷有白色沉淀生成(1分)? Al3++3NH3.H2O ="==" Al(OH)3↓+ 3NH4+ (2分)
本题解析:略
本题难度:一般
4、实验题 某研究性学习小组对过量炭粉与氧化铁(Fe2O3)反应的气体产物成分进行研究。
(1)提出假设 ①气体产物是CO2。?②气体产物是CO。?③气体产物是__________。
(2)设计方案? 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
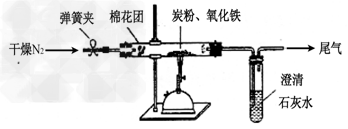
(3)查阅资料氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气,该反应的离子方程式:_______________。
(4)实验步骤
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g; ?
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为_____________。
(5)数据处理试根据实验数据分析判断,前面的假设_________(填①、②、③)是正确的。写出该实验中氧化铁与碳发生反应的化学方程式:______________________。
参考答案:(1)CO2、CO的混合物?
(3)NH4++NO2- N2↑+2H2O
N2↑+2H2O
(4)步骤②中是为了排尽空气、步骤④是为了赶出所有的CO2,确保完全吸收 ?
(5)③;2C+Fe2O3 2Fe+CO↑+CO2↑
2Fe+CO↑+CO2↑
本题解析:
本题难度:一般
5、实验题 学习卤代烃的性质时,王老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH反应生成不同的反应产物,请你一起参与他们的探究。
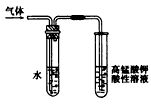
(1)王老师用如上图所示装置进行实验:该实验的目的是_________________;观察到的现象是_________________________;盛水试管(装置)的作用是_____________________________。
(2)若你用另一实验来达到王老师上述演示实验的目的,可以选用另一种溶液代替高锰酸钾酸性溶液。你设计的实验方案依据的反应原理是_____________________(用化学方程式表示)。
(3)小明同学取少量溴乙烷与NaOH水溶液反应后的混合溶液,向其中滴加AgNO3溶液,加热,产生少量沉淀。小明由此得出溴乙烷与NaOH水溶液发生取代反应,生成了溴化钠。老师和同学都认为这样不合理。若请你用实验验证该反应中生成了溴化钠,写出你与小明实验方案的两点不同之处分别是___________________、_______________________。
(4)用波谱的方法能方便地检验溴乙烷发生取代反应的产物,根据你学到的研究有机化合物的方法,使用波谱的名称和波谱仪器记录的结果分别是__________________________。
参考答案:(1)验证生成的气体是乙烯(或验证溴乙烷与NaOH发生消去反应的产物);高锰酸钾溶液褪色;除去气体中少量的乙醇
(2)CH2=CH2+Br2→CH2BrCH2Br
(3)先将混合溶液用稀HNO3酸化;向溴乙烷中加酸化的AgNO3溶液进行对比
(4)核磁共振氢谱图,核磁共振氢谱有三个峰,峰面积之比为1:2:3(或红外光谱图,发现-OH键、C-H键、C-O键振动吸收)
本题解析:
本题难度:一般