| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ��������ת��������̣�2020�����°棩(��)
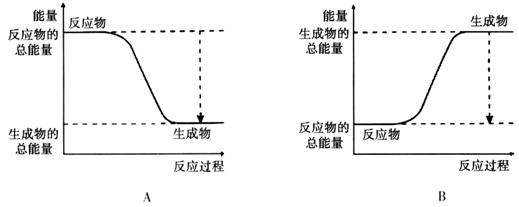 ��3���Ӷϼ��ͳɼ��ĽǶȷ���������Ӧ�������ı仯����֪����ѧ���ļ��ܣ�?
��4����֪1��������ȫȼ������Һ̬ˮ�ų�QKJ��������������ȼ������Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽΪ? ��5������ȼ�ϵ�ص��ܷ�Ӧ����ʽΪ 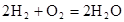 �����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L�� �����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L���ο��𰸣�(1)? ABC?��2��A?��3��484KJ �����������1��A�� ʹ�ô������Դ��ӿ�����Ӧ���ʡ���ȷ��B�� ��Ϊ�����Ƿ�Ӧ����������Ũ�ȣ�������Ӧ���Ũ�ȣ����Լӿ컯ѧ��Ӧ���ʡ���ȷ����ȷ��C�� ��߷�Ӧ���¶ȡ����Լӿ컯ѧ��Ӧ���ʡ���ȷ��D�� ���ͷ�Ӧ���¶ȣ�������ѧ��Ӧ���ʡ�����2��������֪�÷�ӦΪ���ȷ�Ӧ����Ӧ�������������������������ڷ�����Ӧʱ����������ͷų�����ͼ��Ӧ��ΪA����3�����ѻ�ѧ�������������γɻ�ѧ���ͷ���������Ӧ�����е������仯���Ƕ��ߵIJ�ֵ������2molH2��������ȼ��������̬ˮ�ų���������2mol��436kJ/mol+1mol��496 kJ/mol-4mol��463 kJ/mol=484KJ����������ȼ��������̬ˮ���ȷ�Ӧ����ʽΪ2H2 (g)+ O2(g)=2H2O(g)����H=��484KJ/mol�� ��4����Ϊ1��������ȫȼ������Һ̬ˮ�ų�QKJ����������������ȼ������Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽΪ2H2 (g)+ O2(g)=2H2O(l)? ��H=-4QKJ/mol����5��������ȼ�ϵ����ͨ�������ĵ缫Ϊ��������������������Ӧ��n(e-)=0��2mol����n(H2)=0��1mol�� �ڱ�״��������H2�������V=0��1mol��22��4L/mol=2��24L�� �����Ѷȣ�һ�� 3������� ���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮T��ʱ��Ӧ2SO2��g��+O2��g�� �ο��𰸣���1����H=��Ӧ�����յ�����-������ų��������T-E3kJ/mol=-��E2-E1��kJ/mol�� ��������� �����Ѷȣ�һ�� 4��ѡ���� ���ݻ��̶�������ܱ������м���1 mol N2��3 mol H2������Ӧ������������ȷ���� |
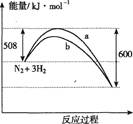
�ο��𰸣�BD
���������A��û�б�ע�����ʵľۼ�״̬������B���ﵽƽ�����������ͨ��1 mol��������������̶����뷴Ӧ��ص����ʣ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�����ȷ��C��ƽ�ⳣ����Ӱ������Ϊ�¶ȣ���С���������ƽ�ⳣ�����䣬����D�������ܽ��ͷ�Ӧ��ܣ���ȷ��
�����Ѷȣ�һ��
5������� ��8�֣���1��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ��?������ȡ����ȡ�����Ӧ��NO2��CO��������?���������������������CO2��NO����������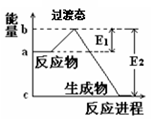
��2����ij���Ϊ2L���ܱ������г���0.5mol NO2��1mol CO����һ�������·�����Ӧ��
NO2+CO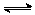 CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.2 mol ����
CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.2 mol ����
�ٸö�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ��Ϊ?��
�ڼ���˷�Ӧ��5 minʱ�ﵽƽ�⣬���ʱ����������������ʵ���Ϊ?��
��������ʵ�ܹ�˵��������Ӧ�ڸ��������Ѿ��ﵽ��ѧƽ��״̬����?
A��������������������ֱ�
B��NO2�����ʵ���Ũ�Ȳ��ٸı�
C�������������ƽ����Է�����������
D��NO2������������CO2�������������
E����������������ʵ������ֲ���
�ο��𰸣���8�֣���1�����ȣ�1�֣�����(1��)��0.05mol/(L��min)(2��)��1.5mol��2�֣���BD��2�֣�
�����������1������ͼ���֪����Ӧ�������������������������������Է�Ӧ�Ƿ��ȷ�Ӧ�����NO2��CO����������CO2��NO����������
��2����������NO�����ʵ���Ϊ0.2 mol������ݷ���ʽ��֪������CO2�����ʵ���Ҳ��0.2mol�����Ըö�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ��Ϊ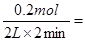 0.05mol/(L��min)��
0.05mol/(L��min)��
���ݻ�ѧ����ʽ��֪����Ӧǰ�����������Dz���ģ����Է�Ӧ��������ܵ����ʵ�����Ȼ��0.5mol��1mol��1.5mol��
����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬������ѡ��B��ȷ�����������غ㶨�ɿ�֪������������������Dz���ģ�����A����ȷ�����ݷ���ʽ��֪����Ӧǰ�����������Dz���ģ�������������������ʵ������ֲ��䣬��E����˵�����������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���ڷ�Ӧ��������������������ʵ����Dz���ģ�C����˵����D�з�Ӧ���ʵķ����෴������������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ��������ȷ�Ĵ�ѡBD��
�������жϻ�ѧƽ��״̬�ı�־�У�(1)�κ�����¾�����Ϊ��־�ģ��٦���=����(ͬһ������)���ڸ���ֺ���(�ٷֺ��������ʵ���������)����ʱ��仯����ij��Ӧ�������(����)���ʡ�ij�����������(����)����=��ѧ������֮�ȣ�(2)��һ�������¿���Ϊ��־���ǣ��ٶ�����ɫ���ʲμӻ����ɵĿ��淴Ӧ��ϵ����ɫ���ٱ仯���ڶ�������̬���ʲμӻ����ɵĿ��淴Ӧ��ϵ������Ӧǰ�������ϵ������ȣ���������ƽ����Է�������M�ͷ�Ӧ��ѹP����(���º���)���۶��ں��¾�����ϵ����ϵ���¶Ȳ��ڱ仯��(3)������Ϊ�жϱ�־���ǣ��ٸ����ʵ����ʵ�����Ũ�ȱ仯��Ӧ����֮��=��ѧ������֮�� (�κ�����¾�����)��������̬���ʲμӻ����ɵķ�Ӧ������Ӧǰ�������ϵ������ȣ���������ƽ����Է�������M�ͷ�Ӧ��ѹP����(���º���)��
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ����ɡ�����٤����.. | |
| �����Ŀ |