1、选择题 向三份0.1mol?L-1CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl2固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
A.减小、增大、减小
B.增大、减小、减小
C.减小、增大、增大
D.增大、减小、增大
2、选择题 下列溶液中离子浓度的关系一定正确的是
A.Na2CO3和NaHCO3溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
B.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的C(H+):
①>②>③
C.等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:2c(K+)=c(X-)+c(HX)
D.pH=3的一元酸HX和pH=11的一元碱MOH等体积混合:c(M+)=c(X-)>c(H+)=c(OH-)
3、选择题 向浓度为0.1 mol・L-1的K2CO3溶液中,分别加入下列物质, 能使c(CO32- )增大的是?
[? ]
A.H2O
B.CO2
C.K2S
D.KOH
4、选择题 Na2CO3 水溶液中存在CO32―+ H2O  ?HCO3―+OH―平衡。下列说法不正确的是
?HCO3―+OH―平衡。下列说法不正确的是
A.稀释溶液,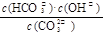 增大
增大
B.通入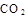 ,溶液pH减小
,溶液pH减小
C.升高温度,此平衡常数增大
D.加入NaOH固体,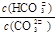 减小
减小
5、选择题
A.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol/L
B.2c(CO32-)+c(HCO3-)+c(OH-)=c(Na+)+c(H+)
C.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.c(CO32-)>c(HCO3-)>c(OH-)>c(H+)