1、填空题 (3分)反应m A+n B p C在某温度下达到平衡。
p C在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是_____________。
②若C为气体,且m+ n = p,在加压时化学平衡发生移动,则平衡必定向______方向移动。
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为_____态。
2、选择题 一定条件下,在密闭容器内,SO2氧化成SO3的热化学方程式为:
 2SO2 (g) + O2 (g) ?2SO3 (g);△H=-a kJ・mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可以是?(?)
2SO2 (g) + O2 (g) ?2SO3 (g);△H=-a kJ・mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可以是?(?)
A.4molSO2和2molO2
B.5molSO2和3molO2
C.4molSO2和4molO2
D.2molSO2、1molO2和2molSO3
3、选择题 在容积一定的密闭容器中,置入一定量的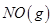 和足量
和足量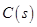 ,发生反应
,发生反应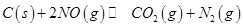 ,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
,平衡状态时NO(g)的物质的量浓度c(NO)与温度T的关系如图所示,则下列说法中,正确的是
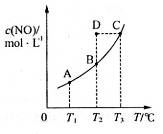
A.该反应的△H>0
B.若该反应在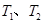 时的平衡常数分别为
时的平衡常数分别为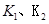 ,则
,则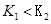
C.在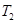 时,若反应体系处于状态D,则这时一定有
时,若反应体系处于状态D,则这时一定有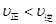
D.在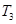 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态
时,若混合气体的密度不再变化,则可以判断反应达到平衡状态
4、填空题 一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH="-196" kJ・mol-1。当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) ΔH="-196" kJ・mol-1。当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是?(填字母)。
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)①SO2的转化率为?;②达到平衡时反应放出的热量为?;③此温度下该反应的平衡常数K=?。?
(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:
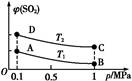
①温度关系:T1?T2(填“>”、“<”或“=”,下同);
②平衡常数关系:KA?KB,KA?KD。
5、选择题 利用下列可逆反应可以将粗镍转化为纯度99.9%的高纯镍:
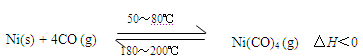
下列说法正确的是
A.50~80℃时,适当增大压强,有利于Ni(CO)4的生成
B.180~200℃时,气态的Ni(CO)4 会分解出纯Ni
C.提纯过程中,CO(g)的量不断减少
D.温度越高,Ni(CO)4 (g)的转化率越低