1��ѡ���� ����Fe��FeO��Fe2O3��ɵĻ�����м���100mL 2mol/L�����ᣬǡ��ʹ�������ȫ�ܽ⣬���ų�448mL���壨S.P.T������ʱ��Һ����Fe3+���������ж���ȷ����?��?��

A����������������ʷ�Ӧʱ������������ʵ���֮��Ϊ1:1:3

B����Ӧ��������Һ�е�Fe2+��Cl�C�����ʵ���֮��Ϊ1:3

C��������У�FeO�����ʵ�����ȷ������Fe��Fe2O3�����ʵ�����

D��������У�Fe2O3�����ʵ�����ȷ������Fe��FeO�����ʵ�����
�ο��𰸣�C
��������� �����ǡ����ȫ�ܽ⣬����Fe3+������Һ������ΪFeCl2��n(HCl)��0.2mol��n(H2)��0.02mol��n(Fe2+)��0.1mol���ɷ�Ӧ2Fe3+��Fe
�����ǡ����ȫ�ܽ⣬����Fe3+������Һ������ΪFeCl2��n(HCl)��0.2mol��n(H2)��0.02mol��n(Fe2+)��0.1mol���ɷ�Ӧ2Fe3+��Fe 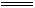 3Fe2+֪Fe��Fe2O3�����ʵ����࣬��FeO�����ʵ�����ȷ����
3Fe2+֪Fe��Fe2O3�����ʵ����࣬��FeO�����ʵ�����ȷ����
�����Ѷȣ�һ��
2������� �ú��������������������ͭ��ȡ�Ȼ�ͭ����CuCl2xH2O������ͼ1������

��֪����pHΪ4��5ʱ��Fe3+������ȫˮ�������������ʱCu2+ȴ������ˮ�⣮
��1����ҺA�еĽ���������Fe3+��Fe2+��Cu2+��������ҺA��Fe2+������Լ�Ϊ______�����ţ���ͬ����
��KMnO4?�ڣ�NH4��2S?��NaOH?��KSCN
��2����������ѡ��______��
��Cl2?��KMnO4?��HNO3?��H2O2
��3��Ҫ�õ��ϴ��IJ�Ʒ���Լ���ѡ��______��
��NaOH?��FeO?��CuO?��Cu2��OH��2CO3
��4������Һ�����ᾧ�õ��Ȼ�ͭ����ķ�����______����ʵ���Ⱥ�˳��ѡ���ţ���
�ٹ���?������Ũ��?����������?����ȴ
��5�����ⶨ��ҺA�е�Fe2+��Ũ�ȣ�ʵ��ǰ������Ҫ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mol������ʱ��Ҫ����������ƽ�����������ձ���ҩ�ס���ͷ�ι��⣬����______����ͼ2�ζ���ʽ�У����������______���гֲ�����ȥ��������ĸ��ţ���
��6��Ϊ�˲ⶨ�Ƶõ��Ȼ�ͭ������CuCl2xH2O��x��ֵ��ij��ȤС�����������ʵ�鷽����
����һ����ȡmg�����������������ټ���Ϊֹ����ȴ������������ˮCuCl2������Ϊn1g��
����������ȡmg��������ˮ��������������������Һ�����ˡ�����ϴ�Ӻ���С��������������ټ���Ϊֹ����ȴ���������ù��������Ϊn2g��?��������������ʵ�鷽����������ȷ�ķ�����______���ݴ˼����x=______���ú�m��n1��n2�Ĵ���ʽ��ʾ����
�ο��𰸣���1���������Ӿ��л�ԭ�ԣ��ܱ������������Ϊ��������ʹ���������ɫ���Ǽ�����ҺA��Fe2+������Լ����ʴ�Ϊ���٣�
��2���������⣬����������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2������Cl2���ʴ�Ϊ���٢ܣ�
��3���õ��ϴ��IJ�Ʒ���Լ���ѡ��CuO��Cu2��OH��2CO3���٢ھ��������������ӣ��ʴ�Ϊ���ۢܣ�
��4������Һ�����ᾧ�õ��Ȼ�ͭ���壬����Ҫ��������Ũ������ȴ���ٽ�֮���˼��ɣ��ʴ�Ϊ���ڢܢ٣�
��5������һ�����ʵ���Ũ�ȵ�KMnO4��Һ��Ҫ�������У���ƽ�����������ձ�����ͷ�ιܡ�250mL����ƿ��������ؾ���ǿ�����ԣ����������ʽ�ζ����У��ʴ�Ϊ��250mL����ƿ��b��
��6��CuCl2?xH2O��x��ֵ��ȷ�������Ǽ���ǰ��������Ϊ���ٵ�ˮ������������ѡ����������CuԪ���غ㣬��
CuCl2?xH2O��Cu��OH��2��CuO��
?1? 1
m135+18x? n280
��?m135+18x=n280
���x=80m-135n218n2��
�ʴ�Ϊ������80m-135n218n2��
���������
�����Ѷȣ�һ��
3������� (NH4)2Fe(SO4)2��6H2O����Ħ���Σ��۸���ˣ���������ˮ������ȱ����ƶѪ�ȣ���һ����Ҫ�Ļ���ԭ�ϡ�
��1��Ħ���ε�ˮ��Һ��?ɫ��
��2��c(Fe2+)��ͬ��Ħ���κ�������������Һ�Ƚϣ����ʵ���Ũ�Ƚϴ����?��
��3��������λͬѧ��ⶨһƿĦ���εĴ��ȡ���ͬѧ��Ƶ�ʵ��װ����ͼ1��
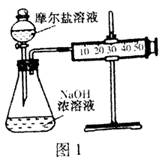
����ͼ�ƶϼ�ͬѧ��ͨ���ⶨ?����Ħ���εĴ��ȡ��÷����IJ���֮������?��
��4����ͬѧ�ڼ�ͬѧ�Ļ��������˸Ľ�����ʵ��װ����ͼ2��
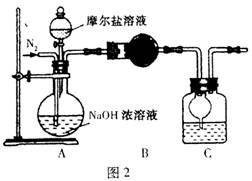
��B��C�е��Լ��ֱ���?��?��C�и���ܵ�������?����ͬѧ��ȡ��10.0g��Ħ������Ʒ����ʵ����Ϻ���ϴ��ƿ��ƿ����Һ������O.68 g�������������������Ħ���εĴ���Ϊ?��(�𰸾�ȷ��С������һλ)��
�ο��𰸣�
��1��dz�̡���2�֣�
��2������������2�֣�
��3�����ɰ���������������֣���
������һ���ֻ��ܽ�����Һ�У��������������ͣ������֣�
��4����ʯ�ҡ���2�֣�?ϡ���ᣨ2�֣�?��ֹ������2�֣�? 78.4��2�֣�
�����������1��Ħ����(NH4)2Fe(SO4)2��6H2O���Ļ��ϼ�Ϊ+2�ۣ�ˮ��ҺΪdz��ɫ����2��ˮ��Һ����������ˮ�⣬��Ħ������笠�����ˮ��������������ˮ�⣬��ͬŨ�ȵ�����Һ����������Ũ�ȸߣ�������c(Fe2+)��ͬ��Ħ���κ�������������Һ�Ƚϣ����ʵ���Ũ�Ƚϴ����������������3��Ħ������笠�������ǿ�Ӧ���ɰ�����ʵ��ⶨ�������������Ħ���ε�Ũ�ȣ�����������ˮ��ʹ�����İ���������ȫ�ݳ�����4����ʵ����ͨ���ⶨ���ɰ����������ⶨĦ���εĴ��ȣ���Ӧ�ȳ��������е�ˮ��������������Һ���գ���Ϊ���������ܽ���ˮ������������������θ���ܷ�ֹ��
n((NH4)2Fe(SO4)2��6H2O)="1/2" n(NH3)=0.68��17��2=0.02mol
m((NH4)2Fe(SO4)2��6H2O)= 0.02��392=7.84g
����Ϊ7.84��10.0=0.784
�����Ѷȣ�һ��
4������� ����Ũ�ȸ�Ϊ2 mol/L��FeCl3��FeCl2��CuCl2�����Һ100 mL������һ���������ۣ������������ա�
��1����ַ�Ӧ��������ڣ�����Һ��һ�����еĽ�����������?��
��2����Ӧ��Ϻ�������ʣ�࣬�������õĹ�������Ϊ?����Һ��һ�����еĽ������ӵ����ʵ���Ϊ?mol��
��3����Ӧ��ϣ��й���ʣ�࣬��Ӧ�����Һ��һ���еĽ���������Ϊ?�������ʵ���ȡֵ��Χ��?��
�ο��𰸣���1�� Fe2����Cu2��?��2�� Cu��Fe �� 0��7 ��3�� Fe2����0��5 mol<n��Fe2������0��7 mol
�����������
�����Ѷȣ�һ��
5��ѡ���� ��һ�������۷����Ȼ�����Һ��,��ȫ��Ӧ��,������Һ��n(Fe2+): n(Fe3+)=1:2.���ѷ�Ӧ��Fe3+��δ��Ӧ�� Fe3+�����ʵ���֮��Ϊ
A��1:2
B��1:3
C��2:3
D��3:2
�ο��𰸣�B
�����������
�����Ѷȣ���