| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《铁的氧化物》高频考点特训(2020年练习版)(十)
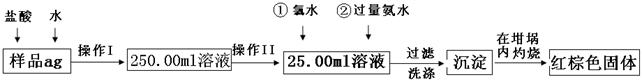 ⑵再加入氨水的离子方程式为?。 ⑶检验沉淀是否洗涤干净的操作是 ?。 ⑷将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1―b2=0.3,则接下来还应进行的操作是?。 ⑸若坩埚的质量为W1g,坩埚与加热后固体的总质量为W2g,则样品中铁元素的质量分数是?。 ⑹有学生认为上述实验步骤太繁琐,他认为,将样品溶于水后充分搅拌,在空气中加热蒸干燃烧称量即可,请你评价是否可行??。(填“可行”或“不可行”) 参考答案:⑴250ml容量瓶(1分) D(1分)⑵Fe3++3NH3H2O = Fe(OH)3↓+3NH4+(2分) 本题解析:(1)根据配制原理可知,还缺少250ml容量瓶。操作II是准确量取溶液的,所以应该用滴定管,答案选D。 本题难度:一般 2、选择题 把铁片放入下列溶液中,铁片溶解且固体的总质量减小,并伴有气体产生,则该溶液是(?) 参考答案:A 本题解析:铁和稀硫酸反应生成硫酸亚铁和氢气,符合题意;铁和硫酸铜反应生成氯化亚铁和铜,该题质量增加;铁和硫酸钠不反应,在浓硫酸中发生钝化,均不符合题意,答案选A。 本题难度:简单 3、选择题 铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98? g(用精密天平测量)Cu(OH)2固体,将其加热有铜的氧化物生成,其质量随温度变化的曲线如图1所示。 参考答案:D 本题解析:A、由0.98? g? Cu(OH)2可知其物质的量为0.01? mol,若全部生成CuO,则质量为0.01? mol×80? g?mol-1=0.8g,所以A点是CuO;若全部生成Cu2O,则质量为0.005? mol×144? g?mol-1=0.72g,所以B点是Cu2O,故A不正确;B、根据化学方程式4Cu2O 本题难度:一般 4、实验题 (14分)Fe在地壳中的含量虽次于铝,但铁及其化合物在生活、生产中的应用最广泛。请回答下列问题: |
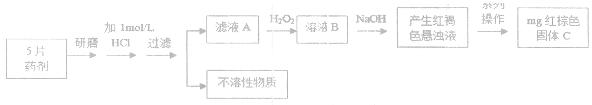
 时间置于空气中,表面“发黄”,请用化学方程式表示原因?。
时间置于空气中,表面“发黄”,请用化学方程式表示原因?。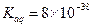 试计算该物质沉淀完全所需要的pH=?(要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)
试计算该物质沉淀完全所需要的pH=?(要求保留2位有效数字)(已知溶液中离子浓度小于10-5mol/L时,该离子可看做沉淀完全,lg2=0.3)参考答案:
本题解析:略
本题难度:一般
5、填空题 (16分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 ==6SO2+Fe3O4,氧化产物为?,若有3 mol FeS2参加反应,
==6SO2+Fe3O4,氧化产物为?,若有3 mol FeS2参加反应,
转移?mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为?。
(3)与明矾相似,硫酸铁也可用作净水剂,其原理为?(用离子方程表示)?
(4)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式?。
(5)铁红是一种红色颜料,其成分是Fe2O.3将一定量的铁红溶于160ml5 mol・L―1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为?。
参考答案:(1)SO2、Fe3O4? 32?(2)2Fe3++Cu=2Fe2++Cu2+?(3)Fe3++3H2O  Fe(OH)3胶体+3H+
Fe(OH)3胶体+3H+
(4)①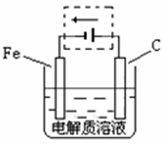 ?②O2+2H2O+4e-=4OH-?(5)11.2g
?②O2+2H2O+4e-=4OH-?(5)11.2g
本题解析:(1)根据方程式可知,FeS2中Fe和S的化合价分别从+2价升高到+8/3价和从-1价升高到+4价,所以FeS2是还原剂,SO2和四氧化三铁都是氧化产物;若有3 mol FeS2参加反应,转移电子的物质的量是(2+6×5)=32mol。
(2)铁离子具有氧化性,能氧化单质铜,方程式2Fe3++Cu=2Fe2++Cu2+。
(3)硫酸铁溶于水电离出的铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,所以可作净水剂,方程式为Fe3++3H2O  Fe(OH)3胶体+3H+。
Fe(OH)3胶体+3H+。
(4)①该装置是铁的电化学腐蚀,所以要保护铁,则可以通过外接电流的阴极保护法,即铁和电源的负极,作阴极,碳和电源的正极相连,作阳极,如同所示。
②原电池中负极失去电子,正极得到电子,所以正极反应式是O2+2H2O+4e-=4OH-。
(5)盐酸是0.8mol,生成的氢气是0.1mol,所以和氧化铁中氧元素结合的氢原子是0.6mol,因此氧化铁是0.1mol,生成0.2mol氯化铁。0.2mol氯化铁消耗铁是0.1mol,生成氢气消耗铁是0.1mol,所以参加反应的铁是0.2mol,质量是11.2g。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《无机非金属.. | |