1、填空题 下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
| 冷轧含锌
废水水质
| 经处理后的水国
家环保标准值
|
Zn2+浓度/(mg・L-1)
| ≤800
| ≤3.9
|
pH
| 1~5
| 6~9
|
SO42-浓度/(mg・L-1)
| ≤23 000
| ≤150
|
经某一工艺处理后的废水pH=8,常温下,该废水中Zn2+的浓度为 mg・
L-1(常温下,Ksp[Zn(OH)2]=1.2×10-17), (填“符合”或“不符合”)国家环保标准。
参考答案:(1)0.78 符合
本题解析:Ksp[Zn(OH)2]=c(Zn2+)・c2(OH-),c(Zn2+)=Ksp[Zn(OH)2]/c2(OH-),c(OH-)=10-14/10-8=10-6(mol・L-1),代入表达式中,得c(Zn2+)=1.2×10-17/(10-6)2=1.2×10-5(mol・L-1),即1.2×10-5 mol・L-1×65×103 mg・mol-1=0.78 mg・L-1,对照表中的数据知,c(Zn2+)<3.9 mg・L-1,故符合标准。
本题难度:一般
2、选择题 已知常温下:Ksp[Fe(OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31;Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=5.6×10-12.某溶液中有浓度均为0.0l?mol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,加入氢氧化钠溶液,当溶液的pH=6时,下列叙述不正确的是( )
A.Fe3+?已经沉淀完全
B.Cr3+已经沉淀完全
C.Zn2+?已经开始沉淀
D.Mg2+还没开始沉淀
参考答案:A、Q(Fe(OH)3)=c(Fe3+)c3(OH-)=0.01×(10-8)3=10-26>Ksp[Fe(OH)3]=2.6×10-39;说明生成氢氧化铁沉淀;依据Ksp[Fe(OH)3])=c(Fe3+)c3(OH-)=2.6×10-39;离子全部沉淀溶液中的铁离子为10-6,计算c(OH-)=32.6×10-3910-6
本题解析:
本题难度:简单
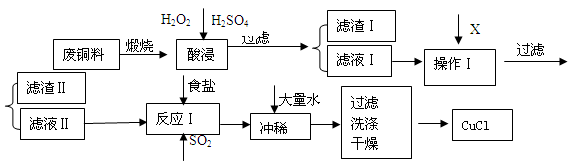
3、简答题 (14分) CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
物质
| 开始沉淀
| 沉淀完全
|
Fe(OH)3
| 2.7
| 3.7
|
Cu(OH)2
| 5.6
| 6.7
|
Al(OH)3
| 3.8
| 4.7
|
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是: 。
(2)操作Ⅰ为调节溶液的PH值,范围为 ,加入的物质X可以是( )
A、CuO B、Cu(OH)2 C、NaOH 溶液 D、CaCO3
(3)滤渣Ⅱ的主要成分是 。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式: 。
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是: 。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为: 。
CuOH + H+的平衡常数为: 。
参考答案:(1)使铜转化为可溶于酸的氧化物 (2)4.7≤PH<5.6 ABC(3)Fe(OH)3 和Al(OH)3
(4)2H2O+2Cu2++SO2+4Cl-="2" CuCl2-+ SO42-+4H+ (5)提高的CuCl2―生成速率 (6)1
本题解析:(1)煅烧的主要目的是使铜转化为可溶于酸的氧化物。(2)操作Ⅰ为调节溶液的PH值,要想溶液中加入的物质消耗H+,同时不引入新的杂质离子,对后边的形成CuCl沉淀有利的物质,应该是CuO、Cu(OH)2、NaOH 溶液。因此选项为A、B、C。调整溶液的pH的范围应该是使杂质离子形成沉淀除去而Cu2+留在溶液中,根据表格提供的数据,应该在4.7~5.6。(3)此时产生的滤渣Ⅱ的主要成分是Fe(OH)3 和Al(OH)3;(4)往滤液Ⅱ中加入食盐并通入SO2发生氧化反应反应,可生成CuCl2-,该反应的离子方程式是2H2O+2Cu2++SO2+4Cl-="2" CuCl2-+ SO42-+4H+;(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是提高的CuCl2―生成速率;(6)因为在常温下,已知CuOH的KSP为1.0×10-14,所以c(Cu+)=1.0×10-14÷10-7=10-7mol/L;Cu++H2O  CuOH + H+的平衡常数为
CuOH + H+的平衡常数为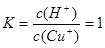 .
.
考点:考查生产CuCl的反应原理、操作方法、实验条件的选择、离子方程式的书写、沉淀溶解平衡的应用。
本题难度:困难
4、选择题 一定温度下,溴化银在水中的沉淀溶解平衡曲线如下图。下列说法正确的是
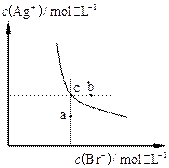
A.向溴化银的浊液中加入溴化钠溶液,
溴化银的Ksp减小
B.图中a点对应的是不饱和溶液
C.向c点的溶液中加入0.1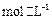
 ,则
,则 减小
减小
D.升高温度可以实现c点到b点的转化
参考答案:BC
本题解析:略
本题难度:一般
5、选择题 在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:
Ca(OH)2(s)  Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
A.c(Ca2+)增大
B.c(Ca2+)不变
C.c(OH-)增大
D.Ca(OH)2固体的质量不变