1、选择题 下列关于弱电解质的说法正确的是:?(?)
A.电解质越弱,则其溶液的导电能力就越差
B.同一弱电解质,浓度越大,电离程度越大
C.升高温度,弱电解质的电离程度减小
D.弱电解质的相对强弱可由相同温度下的电离常数值的大小来判断
2、填空题 (18分)
Ⅰ.(7分)次磷酸(H3PO2)是一种一元中强酸,具有较强的还原性。试回答下列问题:
(1)P的原子结构示意图为 ;
(2)NaH2PO2为 (填“正盐”或“酸式盐”),溶液中有关离子浓度从大到小的顺序为 。
(3)H3PO2可将溶液中的银离子还原为银单质,若氧化剂与还原剂的物质的量之比为4
3、填空题 pH=12的氢氧化钠溶液稀释100倍后,pH=
4、选择题
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋酸分别与锌反应的速率一样大
5、填空题 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH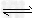 CH3COO-+H+?ΔH>0。
CH3COO-+H+?ΔH>0。
(1)常温常压下,在?pH?=5的稀醋酸溶液中,c(CH3COO-)=____________;下列方法中,可以使0.10?・L-1?CH3COOH的电离程度增大的是______________?
a.加入少量0.10?mol・L-1的稀盐酸?
b.加热CH3COOH溶液
c.加水稀释至0.010?mol・L-1?
d.加入少量冰醋酸
e.加入少量氯化钠固体?
f.加入少量0.10?mol・L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V盐酸_________V醋酸?,反应的最初速率为:υ盐酸_________υ醋酸。
(3)常温下,向体积为Va?mL,pH为3的醋酸溶液中滴加pH=11的NaOH溶液Vb?mL至溶液恰好呈中性,则Va与Vb的关系是:__________________;溶液中各离子的浓度按照由大到小排序为___________________________________.已知:90℃时,水的离子积常数为Kw?=?38×10-14,在此温度下,将pH=3的盐酸和pH?=?11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=______________(保留三位有效数字)。