1、选择题 常温下,Ksp(CaSO4)=9?10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是
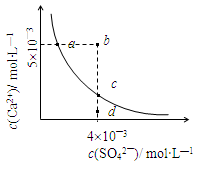
A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42―)对应于曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42―)等于3?10-3 mol・L―1
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
参考答案:D
本题解析:A.常温下CaSO4饱和溶液中,对应c(Ca2+)=c(SO42―)=3?10-3 mol・L―1的这一点,不正确
B:B点溶液中离子积大于9×10-6,所以一定有沉淀析出。由于起始时c(SO42-)小于c(Ca2+),所以平衡时c(SO42-)仍然小于c(Ca2+),即c(SO42-)小于3×10-3 mol/L,B不正确
C:蒸发过程中c(SO42-)应该是增大的,所以选项C不正确。
D:溶度积常数只与温度有关系,所以选项D正确
答案为D
本题难度:一般
2、选择题 一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的溶度积。25 ℃时,在AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下:
物质
| AgCl
| AgI
| Ag2S
|
颜色
| 白
| 黄
| 黑
|
Ksp(25 ℃)
| 1.8×10-10
| 1.5×10-16
| 1.8×10-50
|
下列叙述不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25 ℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
D.25 ℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
参考答案:C
本题解析:由于在25 ℃时AgCl、AgI、Ag2S的溶度积常数不同,在各饱和溶液中Ag+的浓度分别为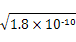 ?mol/L、
?mol/L、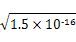 ?mol/L和
?mol/L和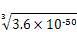 ?mol/L,C不正确。
?mol/L,C不正确。
本题难度:一般
3、填空题 (4分)工业制备氯化铜时,将浓盐酸加热至80 ℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题:
(1)第一步除去Fe2+,有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是 (填代号)。
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当? (填“是”或“否”),理由是 。
(2)除去溶液中Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有 。(多选)
A.NaOH
B.氨水
C.Cu2(OH)2CO3
D.Na2CO3
E.CuO
F.Cu(OH)2
参考答案:(4分)(1)① A ② 否 , 会引入新杂志Na+,造成产品不纯。(2) CEF
本题解析:(1)①NaClO在酸性条件下与Fe2+的反应是:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,由于反应过程中要消耗H+,溶液pH一定升高,选A;②NaClO可以将Fe2+氧化成Fe3+,但引入了新杂质Na+,实际上不能采用,必须应用既能氧化Fe2+又不能引入新杂质的氧化剂,例如Cl2、O2、H2O2等,答案为否 , 会引入新杂志Na+,造成产品不纯;(2)同理,调整pH所选用的试剂可以是CuO、Cu2(OH)2CO3、Cu(OH)2等不会引入新杂质的物质,选CEF。
考点:考查盐的水解,离子除杂等知识。
本题难度:一般
4、选择题 下列有关叙述正确的是
A.高温下进行的反应都是吸热反应,常温下能够进行的反应都是放热反应
B.实验室用4mol SO2与2mol O2进行下列反应:2SO2(g)+O2(g)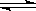 2SO3(g)ΔH=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为80%
2SO3(g)ΔH=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为80%
C.常温下,向纯水中通入一定量二氧化硫,则水的电离平衡被促进
D.向3mL0.1mol/LAgNO3溶液中滴入5滴0.1mol/L NaCl溶液产生白色沉淀,再滴入KI稀溶液沉淀显黄色,则KSP(AgI)<KSP(AgCl)
参考答案:B
本题解析:A项:吸热反应、放热反应的依据与反应条件无关,只与反应前后总能量的大小有关,如果反应物的能量比生成物的能量高则放热,相反是吸热,故A错。C项:酸、碱都会抑制水的电离,二氧化硫通入到水中生成亚硫酸抑制水的电离,故C错。D项:由AgCl转化为AgI,说明KSP(AgI)>KSP(AgCl),故D错。故选B。
点评:知识点多且基础,主在考查学生对基础知识的掌握。影响水电离的因素1.温度。升温总是促进水的电离;2.酸,碱。强酸强碱(强电解质)总是抑制水的电离,弱酸弱碱(弱电解质)也抑制水的电离;3.能水解的盐,盐类(除酸式盐之外)总是促进水的电离;4.活泼金属。因为活泼金属总是与水店里出的氢离子反应,使氢离子浓度减小,所以总是促进水的电离。
本题难度:简单
5、选择题 为除去MgCl2酸性溶液中的Fe3+,不可以使用的试剂是(已知:Mg(OH)2的Ksp:5.6×10?-12,Fe(OH)3的Ksp:4.0×10?-38?)( )
A.NH3?H2O
B.MgO
C.Mg(OH)2
D.MgCO3
参考答案:A、加入NH3?H2O会使铁离子沉淀和镁离子沉淀,起不到提纯的作用,故A不用;
B、加入MgO发生的反应为MgO+2H+=Mg2++H2O,氢离子浓度减小铁离子水解促进生成氢氧化铁沉淀,不引入新的杂质,故B可以用;
C、加入Mg(OH)2发生的反应Mg(OH)2+2H+=Mg2++2H2O,氢离子浓度减小铁离子水解促进生成氢氧化铁沉淀,不引入杂质,故C可以用;
D、加入MgCO3发生的反应MgCO3+2H+=Mg2++CO2↑+H2O,氢离子浓度减小铁离子水解促进生成氢氧化铁沉淀,不引入杂质,故D可以用;
故选A.
本题解析:
本题难度:简单