微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)实验室用氯化钠固体配制2.00mol・L-1的NaCl溶液220ml
(1)请补充该实验的实验步骤:
①计算,②称量,需要称量NaCl?????克,③溶解,④????????,⑤洗涤,? ⑥???????,⑦ 摇匀。
(2)所需仪器为:容量瓶(规格:??????)、托盘天平、 烧杯,还需要那些玻璃仪器才能完成该实验,请写出:??????? ???????????????。
???????????????。
(3)试分析下列操作对所配溶液的浓度有何影响。(填空:A---偏高、B---偏低、C---无影响,填序号)
①定容时,俯视液面。对所配溶液浓度的影响:??????????
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响?? ???????。
???????。
③配制前容量瓶用水洗涤后未 进行干燥处理__________。
进行干燥处理__________。
参考答案:(共8分)?
(1) 29.3. (1分),转移(1分
本题解析:略
本题难度:一般
2、实验题 某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有____________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是_______________________________;
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是____________________________ ;
?(4)要加快上述实验中气体产生的速率,还可采取的措施有_______________________(答两种);
?(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。

①请完成此实验设计,其中:V1=__________,V6=_______???V9=__________,
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈_____________色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因____________________________________。
参考答案:(1)Zn+CuSO4=ZnSO4十Cu、Zn+ H2SO4
本题解析:
本题难度:一般
3、实验题 小军在实验室里做了下列实验:
①分别向盛有稀硫酸和稀盐酸的试管中,滴加紫色石蕊试液;②向盛有稀硫酸的试管中,滴加氢氧化钠试液;③向盛有锌粒的试营中,分别滴加稀盐酸和稀硫酸;④将一根生锈的铁钉分别放入盛有稀盐酸和稀硫酸的试管中,过一会儿取出。
他在纸上记录了以下现象:
a. 溶液没有明显现象;b. 溶液变为黄色;c. 溶液显红色;d. 产生气泡,溶液无色。
下面请你来整理完成实验报告。
(1)实验目的:探究__________(填写物质类别)的化学性质。
(2)实验现象:产生a现象的实验所对应的一类反应通常被我们称作__________反应(该反应属于复分解反应)。
(3)上题所涉及的这类反应在日常生活和工农业生产中有广泛的应用。请举出一个利用该反应的实例:______________________________。
参考答案:(1)酸?(2)中和?(3)用熟石灰改变酸性土壤
本题解析:(1)酸的通性包括与指示剂作用、与碱反应、与活泼金属反应、与碱性氧化物反应等,恰好与小军设计的实验相对应,因此,小军设计该实验的目的是探究酸的性质。(2)上述实验与现象的对应关系是:①――c;②――a;③――d;④――b。(3)中和反应不仅在中学化学中是一类非常重要的反应,在日常生活和工农业生产中也有广泛的应用,如用熟石灰改变酸性土壤、用废碱中和工业污水中的酸等。
本题难度:简单
4、实验题 (12分)用含少量铁的氧化铜制取氯化铜晶体(CuCl2・xH2O)。有如下操作:
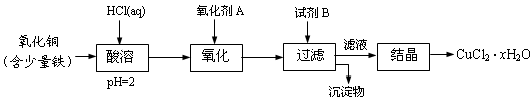
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)氧化剂A可选用_______(填编号,下同)
① Cl2???????????? ② KMnO4??????? ③ HNO3???????? ④ H2O2
(2)要得到较纯的产品,试剂B可选用_______???
① NaOH??????????? ② FeO ???????????? ③ CuO????????? ④Cu2(OH)2CO3
(3)试剂B的作用是______??????
① 提高溶液的pH ② 降低溶液的pH ?? ③ 使Fe3+完全沉淀?? ④ 使Cu2+完全沉淀
(4)从滤液经过结晶得到氯化铜晶体的方法是_________(按实验先后顺序选填编号)
① 过滤???????? ② 蒸发浓缩???????? ③ 蒸发至干???????? ④ 冷却
(5)为了测定制得的氯化铜晶体(CuCl2・xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g。
试评价上述两种实验方案,其中正确的方案是______,据此计算得x = _________(用含m、n的代数式表示)。
参考答案:(12分)(1) ①④(2分)
(2) ③④(2分)<
本题解析:
试题分析:(1)四种试剂都具有强氧化性,为的是制取氯化铜晶体,选用的氧化剂反应后不能生成其它杂质离子,因此选用① Cl2 ④ H2O2。(2)试剂B与氧化剂A选择条件是相似的,因此选用③ CuO④Cu2(OH)2CO3。(3)选择的试剂B,通过与酸的反应生成Cu2+且提高溶液的pH。因在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。所以促使了Fe3+完全沉淀。(4)氯化铜晶体的生成,对滤液先加热蒸发使水份减少溶液浓缩,再冷却结晶,过滤就得到了氯化铜晶体。(5)氯化铜晶体灼烧的温度足以分解氯化铜,氯化铜经过灼烧是不能以氯化铜的形式存在的,会分解为CuO,CuCl2+2H2O Cu(OH)2+2HCl Cu(OH)2
Cu(OH)2+2HCl Cu(OH)2 CuO + H20,固体不可能为纯净的CuCl2,因此第一种方法不正确。第二方案中,最终生成的是CuO,根据铜原子守恒可得:
CuO + H20,固体不可能为纯净的CuCl2,因此第一种方法不正确。第二方案中,最终生成的是CuO,根据铜原子守恒可得:
CuCl2?xH2O → CuO
135+18x ??????80
m ????????????n
(135+18x)/m = 80/n
x=(80m-135n)/18n
点评:解答本题找准考点是关键,考查了盐类水解,注意方案一中最终的固体不可能为纯净的CuCl2。
本题难度:一般
5、选择题 某同学用同一种Mg、Al合金进行甲、乙、丙三组实验,测得如下数据(盐酸的物质的量浓度相等), 下列分析推理不正确的是
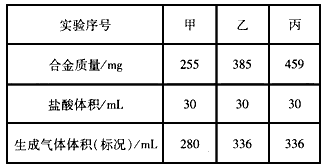 [???? ]
[???? ]
A.甲组实验中盐酸过量
B.乙组实验中盐酸不足
C.合金中Mg、Al的物质的量之比为1:1
D.盐酸的物质的量浓度为3.0 mol
参考答案:D
本题解析:
本题难度:一般