微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (11分)(2011・滨州模拟)Ⅰ.回答下列有关常数的问题:
(1)Kw的数学表达式是________,温度升高Kw________(选填“变大”“变小”或“不变”),若定义pOH=-lgc(OH-),则pH+pOH=________(用含Kw的代数式表示)。
(2)Ka通常表示弱酸的电离平衡常数,Ka值越大表示该弱酸的酸性________。α通常称为电离度,顾名思义是表示弱电解质的电离程度大小的一个指标,对于某一元弱酸,当用蒸馏水稀释该酸时,Ka________(选填“变大”“变小”或“不变”)。α________(选填“变大”“变小”或“不变”)。
(3)Ksp表示难溶物的溶度积常数,该常数越大表示________。
Ⅱ.已知常温下,AgBr的Ksp=4.9×10-13mol2・L-2、AgI的Ksp=8.3×10-17mol2・L-2。
(1)现向含有AgI的饱和溶液中:
①加入固体AgNO3,则c(I-)________(填“变大”“变小”或“不变”,下同);
②若改加更多的AgI,则c(Ag+)________;
③若改加AgBr固体,则c(I-)______;而c(Ag+)______。
(2)有关难溶盐的溶度积及溶解度(与AgBr、AgI无关),有以下叙述,其中正确的是________。
A.两种难溶盐电解质,其中Ksp小的溶解度一定小
B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变
C.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积
D.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀
E.难溶盐电解质的Ksp与温度有关
F.同离子效应(加入与原电解质具有相同离子的物质),使难溶盐电解质的溶解度变小,也使Ksp变小
(3)现向含有NaBr、KI均为0.002 mol・L-1的溶液中加入等体积的浓度为4×10-3 mol/L AgNO3溶液,则产生的沉淀是________(填化学式);若向其中再加入适量的NaI固体,则最终可发生沉淀转化的总反应方程式表示为:______________________________。
2、填空题 (12分)皮革工业污泥中含较多的Cr,工业采用以下工艺制得M[Cr(OH)(H2O)5SO4]。
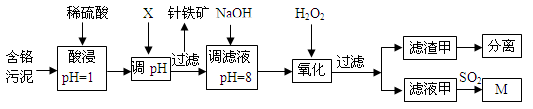
已知:①工艺中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+。
②常温下部分阳离子以氢氧化物沉淀形式存在时溶液的pH见下表:
阳离子
| Fe3+
| Al3+
| Cu2+
| Mg2+
| Cr3+
|
开始沉淀时的pH
| 1.9
| 3.7
| 4.7
| 9.3
| ---
|
沉淀完全时的pH
| 3.2
| 8.0
| 6.7
| 11.1
| 9(>9溶解)
(1)酸浸时,为了提高浸取效率可采取的措施是________________(任写一条)。
(2)调节pH所用X可以选用 。
A.NaOH B.Na2CO3 C.H2SO4 D.HNO3
(3)加入H2O2 目的是把Cr(OH)3沉淀转化为Cr2O72-,写出该反应的离子方程式 。针铁矿组成元素是Fe、H、O,化学式量为89,其化学式是______________。
(4)调滤液至pH=8,Al3+、Cu2+、Mg2+中的_________将转化为沉淀。
(5)若滤液甲的pH=a,则溶液中c (Cu2+)= 。(25℃时的Ksp[ Cu(OH)2]=2.2×10-20)
3、选择题 25℃时,Fe(OH)3的Ksp=4×10-38,若使某溶液中Fe3+完全沉淀所需pH最接近
A.3
B.7
C.9
D.11
4、选择题 下列说法正确的是(????)
A.水垢的主要成分是MgCO3和CaCO3
B.硬水的软化是将全部的Mg2+、Ca2+除尽
C.加入FeS、MnS以除去工业废水中的Cu2+、Cd2+、Pb2+等重金属离子
D.胃舒平的主要成份是氢氧化铁,可治疗胃酸过量,同时也可补铁。
5、选择题 已知25℃时3种难溶电解质的溶度积:AgCl?? 1.8 ×10-10;AgI?? 1.5×10-16;Mg(OH)2? 1.8 ×10-11。在25℃上述3种难溶电解质各自的饱和溶液中,下列判断正确的是
A.AgCl饱和溶液中c(Ag+)比AgI饱和溶液中c(Ag+)大
B.AgCl饱和溶液中c(Ag+)比Mg(OH)2饱和溶液中c(Mg2+)大
C.将AgCl与AgI的饱和溶液等体积混合,再加入足量浓AgNO3溶液,则发生的反应为:AgCl与AgI沉淀都有,但以AgI沉淀为主。
D.若往AgCl饱和溶液中加入0.1 mol/LKI溶液,有黄色沉淀产生
|