微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g)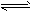 zC(g)(正反应为放热反应);达到平衡后测得A气体的浓度为0.5 mol・L-1;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A的浓度为0.3 mol・L-1。则下列叙述正确的是[???? ]
zC(g)(正反应为放热反应);达到平衡后测得A气体的浓度为0.5 mol・L-1;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A的浓度为0.3 mol・L-1。则下列叙述正确的是[???? ]
A.平衡向右移动
B.x+y>z
C.B的转化率提高
D.C的体积分数增加
参考答案:B
本题解析:
本题难度:一般
2、填空题 X、Y、Z三种短周期元素,其中X元素的原子序数大于Y,且X、Y的氧化物都是形成酸雨的主要物质。Z是地壳中含量最高的金属元素;而地壳中含量最高的非金属元素与X同主族、与Y同周期。
(1)实验室用H2XO4制取XO2气体的化学反应方程式为 。(请用具体元素符号表示化学式,下同)
(2)t℃时,0.1 mol・L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为 。
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式 。
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g)  Y2O3(g),其平衡常数表达式为K= 。
Y2O3(g),其平衡常数表达式为K= 。
(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H=-905.8kJ・mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ・mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为 。
参考答案:
(1)Na2SO3+H2SO4=Na2SO4+SO2
本题解析:
试题分析:与酸雨有关的两种氧化物为二氧化硫和氮的氧化物,X元素的原子序数大于Y,故XY分别为S和N,Z为Al。(1)实验室中一般用浓硫酸和Na2SO3反应或与铜反应制取二氧化硫;(2)NaHSO3溶液存在HSO3-的电离和水解平衡,根据溶液为酸性,确定以电离为主,故由大到小的顺序为c(Na+)、c(HSO3-)、c(H+)、c(SO32-)、c(OH-);(5)①-②×2得出对应热化学方程式4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1265.8kJ・mol-1
考点:考查物质结构、热化学方程式书写、离子浓度大小比较等有关问题。
本题难度:困难
3、选择题 下列事实中,不能用勒夏特列原理解释的是
A.溴水中有下列平衡:Br2+H2O HBr+HBrO当加入AgNO3(s)后溶液颜色变浅
HBr+HBrO当加入AgNO3(s)后溶液颜色变浅
B.2NO2(g)  N2O4(g) (正反应放热),升高温度可使体系颜色加深
N2O4(g) (正反应放热),升高温度可使体系颜色加深
C.反应CO+NO2 CO2+NO(正反应放热),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应放热),升高温度可使平衡向逆反应方向移动
D.合成氨反应N2+3H2 2NH3(正反应放热)中使用催化剂
2NH3(正反应放热)中使用催化剂
参考答案:D
本题解析:
试题分析:如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,这就是勒夏特列原理,该原理适用于所有的平衡体系。向溴水中加入硝酸银,生成溴化银沉淀,溴离子的浓度降低,是平衡向正反应方向移动,溴单质的浓度不断减小,颜色变浅,A可用此原理解释;升高温度,平衡向逆反应方向移动,二氧化氮是红棕色气体,浓度增大,颜色加深,B可用此原理解释;。升高温度,平衡向吸热反应方向移动,故向逆反应方向移动,C可用此原理解释;使用催化剂,只能提高反应速率,平衡不移动,故不能用勒夏特列原理解释,D正确,答案选D.
考点:勒夏特列原理
本题难度:一般
4、填空题 (12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应
2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。则该条件下反应的平衡常数K=????????????????,SO2的平衡转化率=?????????????????。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。则该条件下反应的平衡常数K=????????????????,SO2的平衡转化率=?????????????????。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有??????????(填字母)
A.升高温度
B.降低温度
C.增大压强
D.减小压强 (E)加入催化剂 (G)移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到重要的化工原料,反应的化学方程式为________________________________________________________________。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是______________________。
参考答案:(12分)
(1)1.6×103 L・ mo![]()
本题解析:略
本题难度:简单
5、选择题 在一定温度下,可逆反应A2(g)+B2(g)?

2AB(g)达到平衡的标志是( )
A.A2、B2、AB的浓度不再变化
B.容器中的压强不再随时间变化而变化
C.A2、B2、AB的浓度之比为1:1:2
D.单位时间内生成nmol的A2同时生成2nmol的AB
参考答案:A、容器内各组分的浓度不随时间的变化而变化,就说明了该反应达
本题解析:
本题难度:一般