微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式不正确的是
A.二氧化碳通入足量澄清石灰水中:CO2+Ca2++2OH-
参考答案:
本题解析:
本题难度:困难
2、填空题 硫元素有多种化合价,可形成多种化合物。
(1)常温下用1mol?L-1 100 mL NaOH溶液恰好完全吸收0.1mol SO2气体,此反应的离子方程式为 ;该溶液pH<7的原因是 (结合方程式回答)。以石墨作电极,电解该物质的饱和溶液时,只有一个电极产生气体,写出阳极的电极反应式 。
(2)请按照浓度由大到小的顺序排列0.1mol/LNa2SO3溶液中的离子 。Na2SO3溶液放置于空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”)。
(3)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
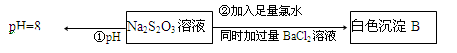
实验①可说明 (填字母)
A.该Na2S2O3溶液中水电离的c(OH―)=10―8mol/L
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3水解方程式为S2O32―+2H2O H2S2O3+2OH―
H2S2O3+2OH―
写出实验②发生反应的离子方程式 。
(4)实验室制得的Na2S2O3粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3・5H2O的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。
称取1.28 g的粗样品溶于水,用0.40mol/L KMnO4溶液(加入适量硫酸酸化)滴定,当溶液中S2O32―全部被氧化时,消耗KMnO4溶液体积20.00 mL。
(5S2O32―+8MnO4―+14H+ =8Mn2++10SO42―+7H2O)。试回答:
①此滴定实验是否需要指示剂 (填“是”或“否”),KMnO4溶液置于 (填“酸式”或“碱式”)滴定管中。
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3・5H2O的质量分数的测量结果会 (填“偏高”“偏低”或“不变”)。
③产品中Na2S2O3・5H2O的质量分数为 。(Na2S2O3・5H2O式量:248)(保留小数点后两位数)
参考答案:(1)SO2+OH―=HSO3―;因有HSO3―存在,HSO
本题解析:
试题分析:(1)由已知:n(NaOH)=1mol?L-1 × 0.1L=0.1mol
n(SO2)=0.1mol,则SO2+OH-=HSO3-;
亚硫酸氢钠溶液呈酸性因为:HSO3-?H++SO32-,HSO3-+H2O?H2SO3+OH-
其中电离程度大于水解程度,故亚硫酸氢钠溶液呈酸性;
以石墨作电极,电解该物质的饱和溶液时,阳极H+放电会生成H2,则阳极无气体应为HSO3-放电,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+;
(2)Na2SO3溶液中,SO32-水解显碱性,离子浓度大小比较为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),Na2SO3溶液放置于空气中一段时间后被氧化:2Na2SO3+O2=2Na2SO4,溶液从碱性变化为中性,pH减小;
(3)由已知:实验①测定溶液pH=8:
A.溶液pH=8,呈碱性,则c水(OH-)=10-6mol/L,故A错误;
B.S2O32-水解显碱性,证明H2S2O3是弱酸,故B正确;
C.Na2S2O3是钠盐为强电解质,故C错误;
D.H2S2O3为二元弱酸,S2O32-水解应分步进行,故D错误;
实验②Cl2将Na2S2O3氧化为Na2SO4,加BaCl2生成BaSO4反应的离子方程式:
S2O32-+5H2O+4Cl2+Ba2+=2BaSO4↓+8Cl-+10H+;
(4)①由于高锰酸钾溶液呈紫红色可作指示剂,当滴入最后一滴溶液呈紫红色,半分钟不褪色,即可指示出滴定终点。因此不需要指示剂。高锰酸钾为强氧化性溶液,可使用酸式滴定管;
②刚看到溶液局部变色就停止滴定,反应并未达到滴定终点,测得的高锰酸钾溶液体积偏低,因此测量结果会偏低;
③n(KMnO4)="0.40mol/L" ×0.020L=0.008mol,则由反应方程式:
5S2O32-+8MnO4-+14H+=8Mn2++10SO42-+7H2O
5 8
n 0.008mol
n=0.005mol
产品中Na2S2O3?5H2O的质量分数=0.005mol×248g/mol/1.28g×100%=96.9%,
考点:了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。了解化学实验是科学探究过程中的一种重要方法。了解化学实验室常用仪器的主要用途和使用方法。能做到设计、评价或改进实验方案。
点评:本题考查了盐类水解应用、离子浓度大小比较、电解原理及应用、氧化还原滴定及指示剂的确定、实验误差分析等知识点,综合性较强,要求学生熟练掌握基础知识,同时要善于进行知识迁移。
本题难度:困难
3、选择题 下列离子方程式书写正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2+ + 2OH- + 2H+ + SO42- = BaSO4 ↓+ 2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH- = NH3 ↑+ H2O
C.次氯酸钙溶液中通入少量二氧化碳:2ClO- + CO2 + H2O =" 2HClO" + CO32-
D.FeBr2溶液中通入过量Cl2:2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl-
参考答案:A
本题解析:略
本题难度:一般
4、选择题 已知电离平衡常数:H2CO3>HClO>HCO,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是
A.向FeI2溶液中滴加少量氯水,反应的离子方程式为2Fe2++Cl2=3Fe3++2Cl-
B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色
C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+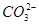
D.能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、Br-能大量共存
参考答案:D
本题解析:A项,应为2I-+Cl2=I2+2Cl-;B项,Fe3+是棕黄色;C项,根据题意应生成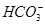 。
。
本题难度:一般
5、填空题 写出下列反应的离子方程式:(每题3分5小题共15分)
(1)石灰石溶于稀盐酸
(2)稀硫酸与氢氧化钡溶液的反应
(3)碳酸钠溶液与硝酸反应
(4)氢氧化铜与稀硫酸反应
(5)向澄清石灰水中通入少量的二氧化碳
参考答案:(1)CaCO3+2H+=Ca2++H2O+CO2
本题解析:略
本题难度:一般