微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (13分)在标准状况下,将224LHCl气体溶于635mL水中(水的密度为1 g/cm3)
所得盐酸的密度为1.18g/cm3,回答下列问题:
(1)该盐酸溶液的质量分数为????????;该盐酸溶液的物质的量浓度为????????。
(2)实验室利用该盐酸来配制250mL0.5mol/L的稀盐酸,从下列用品中选出实验所需要的仪器或用品______________(填序号)
a .胶头滴管?????b.10mL量筒????????c.20mL量筒 ????d. 100mL容量瓶?
.胶头滴管?????b.10mL量筒????????c.20mL量筒 ????d. 100mL容量瓶?
e.玻璃棒???????f.1000mL容量瓶???? g.广口瓶 ???????h.托盘天平
除选用上述仪器外,尚缺少的仪器或用品是__? ______。需取用原盐酸?????????????mL。
(3)下列操作对所配溶液的浓度有何影响?(答偏高、偏低、无影响)
①转移一次后,将洗涤烧杯的残液倒入废液缸中:???????????????。
②定容时仰视容量瓶:?????????。
③定容后,加盖倒转摇匀后观察,发现液面低于刻度线:??? ?????????。
?????????。
2、填空题 (10分)工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾( FeSO4・7H2O )。
(1)若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1:? ▲??。
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为?? ▲??。
(3)硫酸亚铁铵[(NH4)2SO4・FeSO4・6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL? 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V mL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+――Mn2++Fe3++H2O(未配平)
①V的取值范围为???????▲???????????????;
②若V=35,试计算混合物中CuS的质量分数。
3、选择题 下列实验方案合理的是(???? )
A.鉴别甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟
B.检验酒精中的少量水:向酒精中加入足量生石灰
C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应
D.验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液观察是否出现黄色沉淀
4、填空题 亚氯酸钠(NaClO2)是一种重要的消毒剂.已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O,②ClO2的沸点为283K,纯ClO2易分解爆炸,③HClO2在25℃时的电离程度与硫酸的第二步电离程度相当,可视为强酸.如图是过氧化氢法生产亚氯酸钠的工艺流程图:
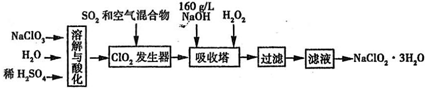
(1)C1O2发生器中所发生反应的离子方程式为______,发生器中鼓入空气的作用可能是______(选填序号).
A.将SO2氧化成SO3增强酸性?? B.稀释C1O2以防止爆炸??? C.将NaClO3氧化成C1O2
(2)在该实验中用质量浓度来表示NaOH溶液的组成,若实验时需要450mLl60g/L的NaOH溶液,则在精确配制时,需要称取NaOH的质量是______g,所使用的仪器除托盘天平、量筒、烧杯、玻璃棒外,还必须有______.
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是______.
(4)在吸收塔中,可代替H2O2的试剂是______?(填序号).
A.Na2O2 B.Na2S?? C.FeCl2 D.KMnO4
(5)从滤液中得到NaClO2?3H2O晶体的实验操作依次是______(填操作名称)
5、选择题 下列各组物质的溶液,分别只用一种试剂一次就可加以区别的是( )
A.Na2SO4、BaC12、K2CO3、KNO3
B.NaAlO2、NaC1、Na2CO3、AgNO3
C.NaOH、KC1、K2CO3、MgCl2
D.HC1、NaNO3、Na2CO3、(NH4)2SO4