微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 2SO2(g)+O2(g)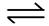 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ・mol-1。
请回答下列问题:
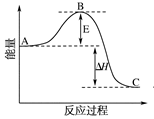
图中A、C分别表示________________、________________,
E的大小对该反应的反应热有无影响?______________。
(2)图中ΔH=____________ kJ・mol-1;
(3) 反应速率v(SO2)为0.05 mol ・ L-1 ・ min-1,则v(O2)=____________mol ・ L-1 ・ min-1、
v(SO3)=____________mol ・ L-1 ・ min-1;
(4) 已知单质硫的燃烧热为296 kJ・mol-1,计算由S(s)生成3 mol SO3(g)的ΔH=________。
参考答案:(1)反应物能量?生成物能量?没有影响? (2)-198?
本题解析:
试题分析:(1)有图可以知道,A为反应物能量,B为生成中间物的能量,C为生成物能量,且E的大小对该反应的反应热没有影响,但是对反应速率有影响,(2)中,1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ・mol-1,所以2SO2(g)+O2(g)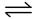 2SO3(g)的
2SO3(g)的
ΔH=-1
本题难度:一般
2、选择题 一定条件下,在容积固定的某密闭容器中发生的反应N2+3H2

2NH3.在10s内N2的浓度由5mol/L降至4mol/L下列说法正确的是( )
A.用NH3表示的化学反应速率为0.1mol/(L?s)
B.使用合适的催化剂,可以加快该反应的速率
C.增加H2的浓度或降低温度都会加快该反应的速率
D.反应足够长时间,N2、H2中至少有一种物质浓度降为零
参考答案:A、10s内v(N2)=
本题解析:
本题难度:简单
3、选择题 已知:4NH3+5O2=4NO+6H2O,若反应速率分别用ν(NH3)、ν(O2)、ν(NO)、ν(H2O)(摩/升?分)表示,则正确的关系是( )
A.
4
5
ν(NH3)=ν(O2)
B.5
6
ν(O2)=ν(H2O)
C.2
3
ν(NH3)=ν(H2O)
D.4
5
ν(O2)=ν(NO)
参考答案:A、由化学反应速率之比等于化学计量数之比,则vO2=
本题解析:
本题难度:简单
4、简答题 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
| 实验编号 | 反应物 | 催化剂
①
10mL2%?H2O2溶液
无
②
10mL5%?H2O2溶液
无
③
10mL5%?H2O2溶液
1mL0.1mol?L-1FeCl3溶液
④
10mL5%?H2O2溶液+少量HCl溶液
1mL0.1mol?L-1FeCl3溶液
⑤
10mL5%?H2O2溶液+少量NaOH溶液
1mL0.1mol?L-1FeCl3溶液
(1)催化剂能加快化学反应速率的原因是______.
(2)常温下5%?H2O2溶液的pH约为6,H2O2的电离方程式为______.
(3)实验①和②的目的是______.实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是______.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
分析上图能够得出的实验结论是______.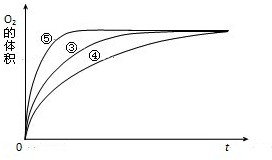
参考答案:(1)催化剂改变反应的途径,降低反应所需的活化能,从而加快反
本题解析:
本题难度:一般
5、填空题 反应A(g)+B(s)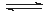 C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:(填增大,减小或不变) C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:(填增大,减小或不变)
(1) 升温___ ; (2) 增大压强____ ; (3) 增大容器容积 ____ ;
(4) 加正催化剂____ ; (5) 加入B____ 。
参考答案:(1)加快 (2)加快 (3)减慢&
本题解析:
试题分析:升高温度,v增大;增大压强,v增大;增大容器容积,压强减小,V减慢;B为固体,加入固体,v不变。
考点:化学反应速率
点评:利用反应速率的公式判断、计算反应速率的大小是高考必考知识点,考生应掌握并灵活应用。
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772
|
|