��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��7�֣�ʵ����������ͼװ�ý����к��ȵIJⶨ����ش��������⣺
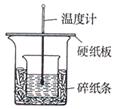
(1)�ڲ�����ȷ��ǰ���£�����к��Ȳⶨȷ�ԵĹؼ���?????
��2����1���������к��Ȳⶨʵ�飬�¶ȼ���ʹ��??????????????????�Σ�ijͬѧΪ��ʡȥ��ϴ�¶ȼƵ��鷳������ʵ��ʱʹ����֧�¶ȼƷֱ������ͼ���¶ȣ����Ƿ�ͬ���ͬѧ�Ĺ۵㣬Ϊʲô��???????????????????????????????????????
��3����Ϊ��ʵ��������ݼ�¼����
2��ʵ���� ij�С��������ͼװ����֤NO�Ļ�ԭ�Լ�̽����ҵ���������ԭ������װ���������Ѽ����ϣ���
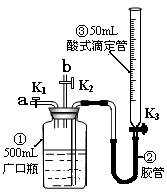
��1������ƿ����ͨ��NO���ⶨNO�����
��ͨ��NOǰ������ƿ���м���ˮ����Ҫ������???????????????��
�ڴӵ���aͨ��һ������NO������¼�ζ��ܶ��������Һ��仯����ֵΪVL��V<50mL����������ѻ���Ϊ��״������ȷ�ⶨNO���������Ҫ������?????????????????????��
��2����֤NO�Ļ�ԭ�ԣ�̽����ҵ���������ԭ��
�١�ֹͣͨ��NO��ر�K1��K3����K2���ӵ���b����ͨ��O2���ɹ۲쵽��������??��д����Ӧ����Ļ�ѧ��Ӧ����ʽ?????????��?????????????��
�ڡ�����ͨ��O2����K3����ʱ�����ζ��ܢ�Һ������ƿ����Һ����ƽ��ֱ�����ƿ���иպó���Һ�塣
i?��ͨ�����������Ϊ1/2Vʱ������ƿ�ٵ��������Ϊ???????????????��
ii �����ƿ���иպó���Һ��ʱ��������Һ�����ʵ���Ũ��Ϊ?????????????mol/L��
3��ʵ���� ����þ�������̼�ķ�Ӧ�Ʋ⣬��Ҳ���ڶ�����̼��ȼ�գ��ҹ���������Ϊ̼���ơ������ơ�̼�е����ֻ����֡�ij��ȤС������ڶ�����̼��ȼ�պ�IJ�����ж��ԺͶ���̽����
��1���������ΪNa2CO3��Na2O��C�Ļ������ʵ�鷽������֤���е�Na2CO3��Na2O���ڴ����д��ʵ�鲽�衢Ԥ������ͽ��ۡ�����֪����ʱBaCO3������Һ��pH=9.6��
��ѡ�Լ���������ϡ���ᡢBaCl2��Һ��Ba(OH)2��Һ������pH��ֽ����ȷ��0.1�����ձ����Թܡ��ιܡ���������������ɫ��
ʵ�����
| Ԥ������ͽ���
|
����1��ȡ����������Ʒ�ڽྻ�ձ��У�������������ˮ����ֽ��裬���ã�ȡ�ϲ���Һ���á�
| �в��ܵĺ�ɫ���塣
|
����2��ȡ��������1��Һ���Թ��У�????
??????????????????????????????????????
| ??????????????????????????????????????
??????????????????????????????????????
|
����3��????????????????????????
????????????????????????????????
| ??????????????????????????????????????
??????????????????????????????????????
?
��2���������ΪNa2CO3��Na2O��C�Ļ���Ϊ��һ���ⶨ������Na2CO3�ĺ���������������ʵ�飺
����1��ȷ��ȡw���������ܽ⡢���˺�ȷ���Ƴ�250mL��Һ��
����2��ȷ��ȡ25.00mL������Һ����ƿ�У��μӼ���ָʾ��A���μ�c mol/L�ı���������Һ��pHԼΪ8.2��̼����Ҫ������ʽΪHCO3�D����������������ΪV1mL���ٵμӼ��μ��ȣ��������������������Һ�ɻ�ɫ���ɫ��������������ΪV2mL��
����3���ظ�ʵ��3�Ρ��ζ��������
�ζ�
����
| ������Һ
�����/mL
| ���ı���������
| V1/mL
| V2/mL
| 1
| 25.00
| 15.02
| 4.97
| 2
| 25.00
| 14.98
| 5.03
| 3
| 25.00
| 13.21
| 6.75
?
�ٲ���2�У���һ���ζ���ʹ�õ�Aָʾ��Ϊ???????????���ζ��յ������Ϊ???????????????????????��
�ڼ���Na2CO3����������=?????????????????���ú�w��c�Ĵ���ʽ��ʾ��
4������� ij��ȤС���ѧ�����ݻ��ý���Mg��CO2������Ӧ���Ʋ���ý�����Ҳ����CO2������Ӧ�������ȤС��������װ�ý��С����������̼��Ӧ����ʵ��̽����β������װ������ȥ������֪�������£�CO��ʹһЩ�������еĽ������ӻ�ԭ
���磺PdCl2 + CO + H2O��Pd��+ CO2 +2HCl ����Ӧ���ɺ�ɫ�Ľ����٣��˷�ӦҲ�����������CO�Ĵ��ڡ�
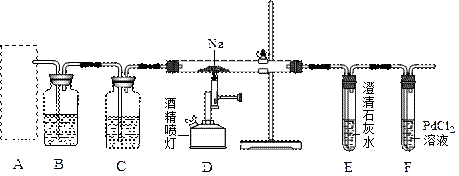
��ش��������⣺?
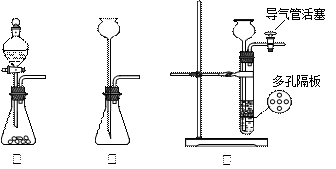
��1��ͨ��ʵ������ȡCO2��������ӷ���ʽ��???????????????????????????????��Ϊ��ʹ����װ���ܡ��濪���ã������ͣ������ͼA��Ӧѡ�õ�װ����___??����д ������������Ҫ��ȡ���������CO2���壬װ��B��Ӧʢ�ŵ��Լ���????????????��Һ��װ��C��Ӧʢ�ŵ��Լ���________??????��
��2���۲�ʵ��װ��ͼ��֪Na��CO2��Ӧ��������_____________�����װ�õ���������ò�װ��ҩƷ���ڵ�ȼ�ƾ����ǰ��������еIJ�����____________________����װ��______����д��ĸ���г���????????????????????����ʱ���ٵ�ȼ�ƾ���ƣ��ⲽ������Ŀ����??????????????????????????????????????��
��3������CO2����Ϊ��������ʵ������зֱ�������¢١������ֲ�ͬ�������������ش����⣺
����װ��F����Һ�����Ա仯��װ��D���������ֹ������ʣ�ȡ�������������������ᷴӦ������ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽ��????????????????????????????????????????????????????????��
����װ��F���к�ɫ�������ɣ�װ��D��ֻ����һ�ֹ������ʣ�ȡ�����ù��������ᷴӦ��Ҳ����ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽ��??????????????????????????????????????????????????????????��
��4���������ּ�Ҫ˵�����жϢ���Dװ�����ɹ���ijɷ����Ƶ����λ���ʽ�ε����ɡ�??????????????????????????????????????????????????????????????????��
5��ʵ���� �ڽ���ijʵ��̽�������У�һЩѧ�����ֵ�������ͭƬ�ֱ�������������������Ũ�����ϡ���ᷴӦ��������Һǰ��Ϊ��ɫ������Ϊ��ɫ��
�����������ѧ���ǽ��������ۺ������������ֹ۵㣺
һ����Ϊ���������Cu2+Ũ�ȵIJ�������ġ���ͬ�����ֿ�����?????(�ͬ�⡱��ͬ�⡱)��ԭ����????????????????????????????????????????????????��
��һ����Ϊ���ʡ���ɫ����Cu2+��NO2��ϵĽ����������Ƴ�һ��ʵ�鷽��֤��֮������Ƶ�ʵ�鷽����???????????????????????????????????????????
��֪0.3mol Cu��������ϡ���ᷴӦ����ԭ��HNO3�����ʵ�����????mol��
|
|