微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
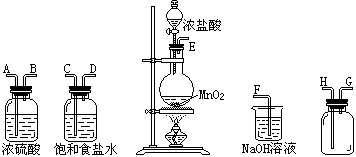
(1)???(2)???????(3)????????(4)????(5)
(1)连接上述仪器的正确顺序是(填各接口处的字母):????接????,_____接????,_____接????,????接????。
(2)在装置中:
①饱和食盐水起的作用是???????????????????????????????,
②浓硫酸起的作用是???????????????????????????????????????;
(3)该实验中收集氯气用的是???????法,若图(2)装满饱和食盐水,也可以用来收集氯气,则收集时氯气应从?????(填“C”或“D”)通入。
参考答案:(1)E接C,D接A,B接H,G接F
(2)洗气??干
本题解析:略
本题难度:简单
2、实验题 (14分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
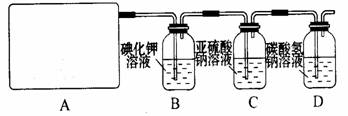
试回答:
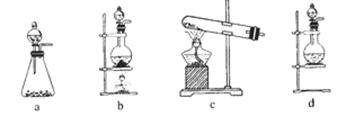
(1)该实验中A部分的装置是 (填写装置的序号)。
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式???????????? 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:取漂白粉适量,研磨后溶解,配制成漂白液,运用下列实验,检测该漂白液的性质。
①将少量漂白液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测漂白液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向漂白液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。
请回答以下问题:
a、实验①表现出该消毒液具有 性;
b、实验②用pH试纸检测消毒液的操作是 _______________________;
c、实验③中涉及反应的离子方程式为 ____________;
参考答案:(14分)
(1)b
(2)取C中溶液少量,加入
本题解析:(1)实验室制氯气是固液加热装置,故选b
(2)Na2SO3被氧化为Na2SO4,故本题的目的是检验硫酸根离子的存在:取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)也就是生成了HClO:Cl2+HCO3-=CO2+Cl-+HClO
(4)氯气有毒,一定要有尾气处理装置
(5)①证明有碘单质的生成,说明消毒液具有氧化性;
②基本的实验操作;
③有氯气的生成:Cl-+ClO- +2H+=Cl2↑+H2O
本题难度:一般
3、实验题 (12分)天然水是人类饮用水的主要来源。从天然水获得可以饮用的水一般须经过沉降悬浮物、杀菌消毒等步骤。
(1)沉降悬浮物要在水中加入絮凝剂,如将铝盐加入水中能达到净水目的,
原因是??????????????(用离子方程式表示)。
(2)氯气可用于自来水杀菌消毒剂,结合离子方程式和文字理由????????????。
(3)新型水处理剂高铁酸钾 (K2FeO4)具有强的氧化作用和絮凝作用。工业上可通过以下流程制备高铁酸钾:
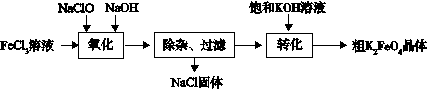
查阅资料:高铁酸盐在中性或酸性溶液中会逐渐分解,在碱性溶液中稳定。
完成“氧化”过程中的离子方程式
□Fe3+ + □ClO- +□??????="□" FeO42- + □Cl- +?□???
“转化”过程中实现由Na2FeO4制得K2FeO4,是利用二者????????性的不同。
③结合资料完成粗K2FeO4晶体的提纯:将粗产品用???????溶解,然后再加入饱和KOH溶液、冷却结晶、过滤。
④高铁酸钾的应用还在不断扩展中。如可制成高铁电池,?电池反应为:
3Zn?+?2K2FeO4?+?8H2O  ??3Zn(OH)2?+?2Fe(OH)3?+?4KOH?
??3Zn(OH)2?+?2Fe(OH)3?+?4KOH?
放电时,正极反应为:????????????。
参考答案:(12分)
(1)Al3++3H2O
本题解析:
试题分析:(1)铝盐加入水中能达到净水目的,是因为铝离子水解得氢氧化铝胶体,具有吸附作用,离子方程式是Al3++3H2O Al(OH)3(胶体)+ 3 H+
Al(OH)3(胶体)+ 3 H+
(2)氯气溶于水生成次氯酸,Cl2 + H2O =" HCl" + HClO,次氯酸具有强氧化性,用来杀菌消毒;
(3)①根据题目的流程图判断反应物中有氢氧化钠,所以反应物的空白处应是OH-,则产物的空白处应是H2O,根据得失电子守恒,配平该化学方程式,答案是2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl- +5H2O??;
②“转化”过程中实现由Na2FeO4制得K2FeO4,是利用二者溶解性的不同,K2FeO4比Na2FeO4的溶解度小;
③高铁酸盐在中性或酸性溶液中会逐渐分解,在碱性溶液中稳定,所以将粗产品用稀KOH溶液溶解;
④放电时,将化学能转化为电能,正极发生还原反应,电极方程式为2FeO42-+6e-+8H2O==2Fe(OH)3+10OH-
本题难度:一般
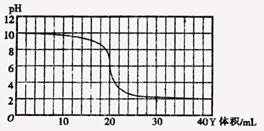
4、选择题 量取20.00mL0.01mol/LX溶液于锥形瓶中,用滴定管逐滴滴入0.01mol/L的Y溶液中,用数字化试验设备测定试验过程中混合液的PH,结果如图所示。下列说法中正确的是?
A.X和Y可能是KOH和CH3COOH
B.X和Y可能是NH3・H2O和HCl
C.X与Y恰好中和时, 混合液呈中性
D.X与Y恰好完全反应时的溶液中滴入酚酞会变色
参考答案:B
本题解析:如果X是强碱,则氢氧化钾的pH=12,A不正确。根据图像可知,恰好反应时,pH=6,溶液显酸性,所以B正确,CD都不正确,答案选B。
本题难度:一般
5、选择题 在配制100mL 2mol/L的NaOH溶液时,下列操作会导致结果偏低的是(?? )
(1)用拖盘天平称量时砝码放在左盘
(2)溶解NaOH固体后没有冷却至室温就向容量瓶转移溶液
(3)将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
(4)定容时俯视刻度线
(5)定容时仰视刻度线
(6)干净的容量瓶未经干燥就用于配制溶液
A.(2)(4)(6)
B.(1)(3)(4)
C.(1)(3)(5)
D.(2)(3)(4)
参考答案:C
本题解析:略
本题难度:简单