��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
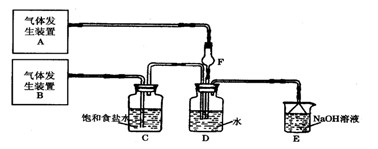
1��ʵ���� ��8�֣�Ϊ��̽��Cl2��SO2ͬʱͨ��H2O�з����ķ�Ӧ��ijУ��ѧ��ȤС��ͬѧ���������ͼ��ʾ��ʵ��װ�á�
����ա�
��1��Dװ������Ҫ��Ӧ�����ӷ���ʽΪ??????????????????????????????????????��
F�����������ǣ�?????????????????????????????????????????????????????��
��2��Ϊ��֤ͨ��Dװ����������Cl2����SO2��������ȤС���ͬѧ���������Լ���
 ?????????�� �Ȼ���ϡ��Һ??? �� �Ȼ�������Һ??? �� ���軯����Һ
?????????�� �Ȼ���ϡ��Һ??? �� �Ȼ�������Һ??? �� ���軯����Һ
�� ������Һ??????? �� Ʒ����Һ??????? �� ���Ը��������Һ
��Cl2������ȡ����D����Һ�μ���ʢ��?????????��ѡ��һ����ţ��Լ����Թ��ڣ��ټ���??????��ѡ��һ����ţ��Լ��������������ǣ�??????????????????????????????��
��SO2������ȡ����D����Һ�μ���ʢ��?????????��ѡ��һ����ţ��Լ����Թ��ڣ������������ǣ�????????????????????????????????????????????��??????????
�ο��𰸣�
��1��Cl2+SO2+2H2O��4H++2Cl�D+S
�����������
�����Ѷȣ���
2��ѡ���� ��18mol/L Ũ��������100 ml 3.0mol/L ϡ�����ʵ�鲽�����£�
�� ��������Ũ��������?? �� ��ȡһ�������Ũ����?????�� �ܽ�???
�� ת�ơ�ϴ��????????????�� ���ݡ�ҡ��
�ش��������⣺
��1������Ũ����������????????????mL ����ȡŨ�������õ���Ͳ�Ĺ����???????��
����������ѡ��? A. 10mL?? B. 25mL?? C. 50mL?? D. 100ml��
��2���ڢ۲�ʵ��IJ�����???????????????????????????????????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????????��
��3���ڢݲ�ʵ��IJ�����???????????????????????????????????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????????��
��4����������������Ƶ�ϡ����Ũ���к�Ӱ�죿����ƫ��ƫС����Ӱ����д��
A. ���õ�Ũ���᳤ʱ��������ܷⲻ�õ�������???????????????
B. ����ƿ������ˮϴ�Ӻ������������ˮ???????????????
C. ���ù����ձ���������δϴ��?????????????????
D. ����ʱ������Һ��Һ����????????????????????
�ο��𰸣���1��16.7 ��3�֣�?? B ��1�֣�
��2������
�����������
�����Ѷȣ���
3��ѡ���� ʵ�����й�������Ʊ�ʵ���в���ȷ����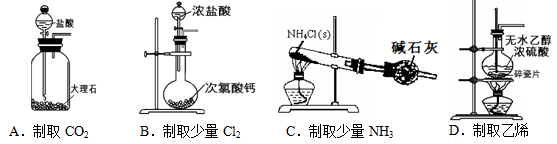
�ο��𰸣�C
���������
�𰸣�C
C��ԭ������ȷ��NH4Cl NH3��HCl����ȴ�����ڴ��Թܿڷ�Ӧ����NH4Cl���壬�ò���NH3
NH3��HCl����ȴ�����ڴ��Թܿڷ�Ӧ����NH4Cl���壬�ò���NH3
�����Ѷȣ���
4��ʵ���� 3λͬѧ���������3��ʵ�鷽������֤ij��ɫ�����мȺ���SO2���ֺ���CO2��
����1������ɫ����ͨ������KMnO4��Һ��KMnO4��Һ��ɫ����Ӧ������ͨ��ʯ��ˮ��ʯ��ˮ����ǡ�����֤ԭ��ɫ�����к���SO2���ֺ���CO2��
����2������ɫ����ͨ����ˮ����ˮ��ɫ��Ӧ������ͨ��ʯ��ˮ��ʯ��ˮ����ǣ�֤��ԭ��ɫ�����мȺ��� SO2���ֺ���CO2��
����3������ɫ����ͨ��Ʒ����Һ��������ͨ���ữKMnO4��Һ��Ʒ����Һ�����ͨ������ʯ��ˮ�����Ʒ����Һ��ɫ��KMnO4��Һ��ɫ��dzƷ����Һ����ɫ��ʯ��ˮ����ǣ�֤��ԭ��ɫ����Ⱥ���SO2���ֺ���CO2��
�Իش�����3�������У���֤��ԭ��ɫ�����м���SO2������CO2�ķ�������???????????????������������???????????????????��
�ο��𰸣���������ʵ������Ӧ�Ƿ���3������SO2���ڡ���SO2��֤��
�������������ʱһҪ����SO2��CO2�Ĺ����Ǿ���ʹ����ʯ��ˮ��룬��Ҫ���ǵ����ߵ�����SO2���л�ԭ�ԣ�����ʹƷ����ɫ��CO2���߱���Щ���ʡ���Ҫ������ʹ����KMnO4��Һ����ˮ��ɫ�����ʲ�����SO2������H2S��C2H4��C2H2�ȡ����֤������SO2����CO2��ʵ�����һ��ӦΪ������SO2���ڡ���SO2��֤��SO2�����ڡ�֤��CO2���ڡ�
�����Ѷȣ���
5��ʵ���� �Ķ��������β��ϣ�
������1785�꣬���ĵ����ڲⶨ�������ʱ����ȥ�����е�O2��N2����֪������������������һ��������������1/200 ��С���ݡ�
��1892�꣬�����ڲⶨ�����ܶ�ʱ���ӿ����еõ��ĵ����ܶ�Ϊ1.2572g/L�� ���Ӻ���������ֽ�õ��ĵ����ܶ�Ϊ1.2508g/L���������0.0064g/L��
����������ķ����ͬ�о�����Ϊ����������ʵ���е� ��С��������ij�ֱ�Ȼ����ϵ����Ԥ������к���ij�ֽ��ص�δ֪���塣������ʵ�飬�������ڷ����˻�ѧ���ʼ������õĶ������塪��벡�
��ش��������⣺
��1�����Ϣ١����еġ�С���Բⶨ������ɺ͵����ܶȵ�ʵ���������Ҫ���ػ��Ǵ�Ҫ���أ�
��2�����Ϣ��п�ѧ��ץס�ˡ�С��������ش���˵����ʲô���⣿
�ο��𰸣���1����Ҫ���أ���2����ѧ�о�Ӧ���Ͻ��Ŀ�ѧ̬�ȡ�
�����������1�� ��С���Բⶨ��������Ҫ�ɷֶ����Ǵ�Ҫ���أ��Ե������ܶ�Ӱ���С��Ҳ�Ǵ�Ҫ���ء����Կ������гɷֵIJⶨ��˵�Ǿ����ܺ��Ե���Ҫ����֮һ����2��ֻҪ�����ͻ�����������ԭ���ҳ���������ԭ���ܻ����ش�ķ��֡���ѧһ��Ҫ�Ͻ���
�����Ѷȣ���