微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
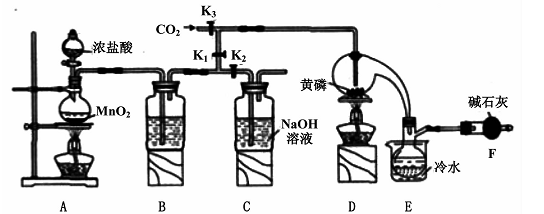
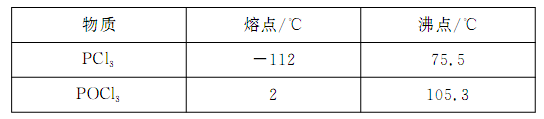
已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3。PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)A装置中制氯气的离子方程式为 。
(2)B中所装试剂是 ,E中冷水的作用是 ,F中碱石灰的作用是 。
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是 。
(4)粗产品中常含有POC13、PCl5等。加入黄磷加热除去PCl5后.通过 (填实验操作名称),即可得到较纯净的PCl3。
(5)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00g产品,加水反应后配成250 mL溶液;
②取以上溶液25.00mL,向其中加入10.00 mL 0.1000 mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000 mol/L的Na2S2O3,溶液滴定
④重复②、③操作,平均消耗Na2S2O3,溶液8.40ml
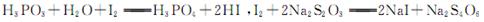 已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。
已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。
参考答案:(1)MnO2+4H++2Cl- 本题解析:
本题解析:
试题分析:(1)二氧化锰和浓盐酸加热制取氯气;(2)干燥氯气用浓硫酸;根据表中PCl3的沸点可得,用冷水可以将其冷凝;根据信息可得PCl3不能遇见水蒸气,还要考虑进行尾气处理,故碱石灰的作用为吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3反应;(3)根据题目信息可知需要排尽装置内的空气;(4)根据题目信息可知利用沸点的不同将混合物分离,故蒸馏;(5)根据碘单质和Na2S2O3的反应求出剩余的碘单质,根据总的碘单质减去剩余的碘单质求出与H3PO3的物质的量,根据磷原子守恒得PCl3的物质的量,从而求出其质量分数。
考点:考察氯气的实验室制法、气体的干燥、根据化学方程式的计算和应用题目信息解题的能力等
本题难度:困难
2、选择题 下列表示物质变化的化学用语正确的是
A.碳酸的电离 H2CO3 2H++CO32-
2H++CO32-
B.氯化铁水解 Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.硫氢化钠的水解 HS-+H2O H3O++S2-
H3O++S2-
D.硫化铝固体在水中不存在 Al2S3+6H2O Al(OH)3+3H2S
Al(OH)3+3H2S
参考答案:B
本题解析:略
本题难度:简单
3、选择题 氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.BrCl+H2O=HCl+HbrO
D.2Na2O2+2H2O=4NaOH+O2↑
参考答案:A
本题解析:
试题分析:反应Br2+SO2+2H2O=H2SO4+2HBr为氧化还原反应,水既不是氧化剂也不是还原剂,A、反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑中水作氧化剂,正确;B、反应4Fe(OH)2+O2+2H2O=4Fe(OH)3中,水既不是氧化剂也不是还原剂,错误;C、反应BrCl+H2O=HCl+HBrO 不是氧化还原反应,水既不是氧化剂也不是还原剂,错误;D、反应2Na2O2+2H2O=4NaOH+O2↑中,水既不是氧化剂也不是还原剂,错误。
本题难度:一般
4、选择题 下列化学用语使用正确的是
A.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(l) △H=―483.6kJ/mol
B.NH4Cl电子式: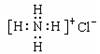
C.苯乙醛结构简式: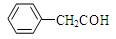
D.丙烷分子的球棍模型:
参考答案:D
本题解析:略
本题难度:一般
5、填空题 按要求写出下列方程式:
(1)一种单质与一种盐发生反应的方程式:______
(2)小苏打电离的电离方程式:______
(3)碳酸钙与盐酸反应的离子方程式:______.
参考答案:(1)一种单质与一种盐发生反应可以是金属与盐的置换反应,如F
本题解析:
本题难度:简单