微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A.11.2L NO和11.2L O2混合后的分子总数为NA
B.1mol苯乙烯中含有的碳碳双键数为4NA
C.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
D.1mol Fe与足量的稀HNO3反应并放出NO和N2O,转移3 NA个电子
参考答案:D
本题解析:
试题分析:A、NO与氧气混合发生反应2NO+O2=2NO2,反应是体积减小的可逆反应,因此11.2L NO和11.2L O2混合后的分子总数小于NA,另外气体的状态也不一定是在标准状况下,A不正确;B、苯环分子中不存在碳碳双键,因此1mol苯乙烯中含有的碳碳双键数为NA,B不正确;C、浓硫酸与铜反应随着反应的进行浓度降低,稀硫酸与铜不反应,所以50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目小于0.46NA,C不正确;D、铁与足量的稀硝酸反应生成硝酸铁,转移3个电子,因此1m
本题难度:简单
2、选择题 下列反应既属于氧化还原反应,又属于化合反应的的是
A.2Fe+3Cl2 2FeCl3
2FeCl3
B.Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
C.CaO+CO2=CaCO3
D.H2SO4+2NaOH = Na2SO4+2H2O
参考答案:A
本题解析:
试题分析:氧化还原反应的特征是有化合价的升降,化合反应是多变一的反应。
本题难度:简单
3、填空题 (6分)根据下列叙述,画出对应1--3的微粒结 构示意图:
构示意图:
(1)A元素原子的最外层电子数为电子层数的3倍:???????????????????。
(2)与Ar原子电子层结构相同的-1价阴离子:???????????????????????。
(3)质量数为23,中子数为12的原子?????????????。
(4)(2分)写出下列物质的名称
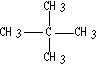 ___________
___________
(5)C5H12的同分异构体有?????????????种
参考答案:略
本题解析:略
本题难度:一般
4、计算题 (9分)1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将17.4gMnO2与200g 36.5%的浓盐酸(过量)完全反应,把反应后所得溶液稀释到400mL。
MnCl2+Cl2↑+2H2O。现将17.4gMnO2与200g 36.5%的浓盐酸(过量)完全反应,把反应后所得溶液稀释到400mL。
(1)请用双线桥表示该反应电子转移方向和总数 _ __。MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)计算生成Cl2的体积(折算成标准状况)为__ ____L(写计算过程,否则不得分)。
(3)计算稀释后溶液中Cl―的物质的量浓度为__ ___ mol・L―1(写计算过程,否则不得分)。
参考答案:20.(9分)
(1) 本题解析:
本题解析:
试题分析:(1)双线桥法表示电子转移,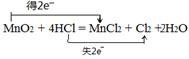 ;
;
(2)17.4gMnO2的物质的量为0.2mol,200g 36.5%的浓盐酸中HCl的物质的量为2mol,Cl-为2moL
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O 反应掉2Cl-
MnCl2+Cl2↑+2H2O 反应掉2Cl-
22.4 2
0.2 V n V=4.48L n=0.4moL
(3)稀释后溶液中Cl―的物质的量浓度为(2-0.4)/0.4=4 mol/L。
考点:考查氧化还原反应电子转移的表示方法,根据化学方程式计算。
本题难度:一般
5、选择题 下列有关化学用语表示正确的是()
A.NH3的电子式:
B.CS2分子的球棍模型:
C.二氧化硅的分子式:SiO2
D.Mg5(Si4O10)2(OH)2?4H2O的氧化物形式:5MgO?8SiO2?5H2O
参考答案:D
本题解析:NH3的电子式为 ,选项A不正确;原子半径小于S原子半径,且二硫化碳是直线型结构,选 91eXAm.org项B不正确。二氧化硅是原子晶体,是由原子构成的,不存在分子,选项C不正确,所以正确的答案选D。
,选项A不正确;原子半径小于S原子半径,且二硫化碳是直线型结构,选 91eXAm.org项B不正确。二氧化硅是原子晶体,是由原子构成的,不存在分子,选项C不正确,所以正确的答案选D。
本题难度:一般