微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将1mol N2和3mol H2通入4L的密闭容器中反应,半分钟后测得H2的物质的量为2.1 mol,现用如下三种物质在单位时间内的浓度变化来表示该反应速率:
① v(H2) = 0.45mol/(L・min) ② v(N2) = 1.05mol/(L・min) ③ v(NH3) = 0.30mol/(L・min) 其中正确的是 [???? ]
A.①②
B.②③
C.①③
D.①②③
参考答案:C
本题解析:
本题难度:简单
2、填空题 某温度下,向某密闭容器中加入1mol氮气和3mol氢气,使之反应合成氨,平衡后,测得氨的体积分数为m。若温度不变,只改变起始加入量,使之反应重新达平衡后,氨的体积分数仍然为m。若氮气、氢气和氨的加入量用x,y,z表示,应满足:
(1)温度、体积恒定时:若x=0,y=0则z=_______。温度、压强恒定时:若x=0,y=0则z_______。
(2)温度、体积恒定时:若x=0.75mol,y_______,z_______。温度、压强恒定时:若x=0.75mol,y_______,z_______。
(3)温度、压强恒定时:x,y,z应满足的关系是__________。
参考答案:
(1)温度、体积恒定时:z=2mol,温度、压强恒定
本题解析:
【错解分析】(1)温度、压强恒定时:z=2mol
(2)温度、压强恒定时:z=0
(3)温度、压强恒定时:y=3x,z=2-2x
【正解】温度、体积恒定时,为了使达到平衡时氨的体积分数保持不变,加入的量必须和初始加入的量相当,即全为反应物应是1mol氮气和3mol氢气;全为生成物应是2mol氨气(若反应物、生成物皆有,折算为上述量)。但遇到温度、压强恒定时,由于思维定势,往往也取相当量,只能得出所有满足条件中的一个特殊情况。
实际上为了满足温度、压强恒定,只需根据体积大小,加入与初始相当的量即可满足题目的要求。如:假设本题的初始体积为VL,加入1mol氮气和3mol氢气,平衡后,测得氨的体积分数为m。而当体积改为2VL时,应加入2mol氮气和6mol氢气(或4mol氨,或其他相当的量),相当于每VL里仍加入1mol氮气和3mol氢气,平衡后,氨的体积分数不变,仍为m;……。因此,z的取值由体积大小而定,若无反应物,z为大于零的任意值;若有反应物,z为大于等于零的任意值。
本题难度:一般
3、填空题 (11分)
(Ⅰ)有可逆反应A(g) + 3B(g)? ??2C(g) △H<0
??2C(g) △H<0
(1)已知该反应的平衡常数表达式:K=[C]2/[A][B]3?;升高温度,平衡常数K将_______________(填“增大”,“减小”,“不变” )。([X]表示相应物质的浓度)
(2)一定条件下,该反应达平衡后,保持其他条件不变,再充入C气体,20 min后又达新平衡。试推测,与原平衡状态相比,第15 min时,V正_______(填“增大”,“减小”,“不变” ),V逆______(填“增大”,“减小”,“不变” )。
(3)该反应的速率与时间的关系如下图所示:
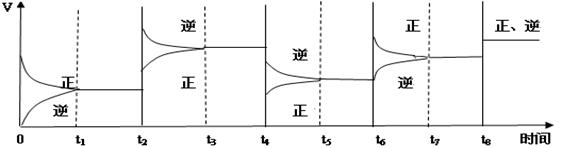
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,请指出改变了什么条件(例如:减小生成物的浓度)
t2时_________??? ___;t4时______?_____;t6时___??_______;t8时_______?____。
(Ⅱ)、一定温度下在体积为5 L的密闭容器中发生可逆反应。
若某可逆反应的化学平衡常数表达式为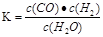
(1)写出该反应的化学方程式:???????????????????????????????????;
(2)能判断该反应一定达到化学平衡状态的依据是???????(填选项编号)。
A.容器中气体的平均相对分子质量不随时间而变化
B.υ正(H2O)=υ逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总的物质的量不随时间而变化
E. 消耗n mol H2的同时消耗n mol CO
参考答案:(1)????减小(1分)????(2)增大????增大??
本题解析:(Ⅰ)(1)反应是放热反应,所以升高温度平衡向逆反应方向移动,平衡常数减小。
(2)增大生成物浓度,正逆反应速率都是增大的。
(3)t2时正逆反应速率都是增大的,但平衡向逆反应方向移动,所以改变的条件是升高温度。t4时正逆反应速率都是减小的,但平衡向逆反应方向移动,所以改变的条件是减小压强;t6时正反应速率增大,逆反应速率不变,平衡向正反应方向移动,所以改变的条件是增大反应物浓度;t8时,正逆反应速率都是增大的,但平衡不移动,所以改变的条件是使用了催化剂,
(Ⅱ)(1)根据平衡常数的表达式可知,方程式为C+H2O(g) H2+CO。
H2+CO。
(2)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以B正确。E中反应速率的方向是相同的,不正确。反应前后条件减小,所以压强也是减小的,D正确。密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但质量是变化的,所以C正确。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量和物质的量都是变化的,所以A可以说明。答案选ABCD。
本题难度:一般
4、简答题 在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
| 0min | 10min | 20min | 30min | 40min | 50min
830℃
1mol
0.8mol
0.65mol
0.55mol
0.5mol
0.5mol
1 100℃
1mol
0.75mol
0.6mol
0.6mol
0.6mol
0.6mol
(1)1100℃时,前10min该反应的化学反应速率v(CO2)=______,830℃平衡后CO转化率的为______.
(2)1100℃时化学平衡常数K=______,该反应为______反应(填“吸热”和“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是______.
(a)容器中压强不变(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡______
______移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H2百分含量______(选填“增大”或“减小”或“不变”).
(5)830℃时,若在体积为2L的密闭容器中充入1molCO2和1molH2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H2)随时间变化而变化的趋势图.
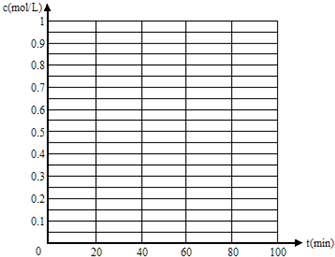
参考答案:(1)v(CO)=
本题解析:
本题难度:一般
5、选择题 在某恒定温度下,向容积为1 L的容器中投入1 mol CO和2 mol H2O,发生如下反应:CO(g)+H2O(g)???CO2(g)+H2(g),平衡时生成CO2 2/3 mol。若保持温度和容积不变,向其中增加2 mol H2O(g),使反应到达新的平衡,下列说法不正确的是(???)
A.新、旧平衡时容器内气体的压强之比是5:3
B.新平衡时H2O的转化率为20%
C.新平衡时CO的浓度是0.2 mol ・L-1
D.新、旧平衡时容器内气体密度之比为5:3
参考答案:D
本题解析:略
本题难度:一般
|