微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下图所示,用石墨作电极进行电解,电解槽甲中盛AgNO3溶液,电解槽乙中盛有含二价金属G的氯化物溶液1 L,其物质的量浓度为0.1 mol・L-1,当通电一段时间后,电解槽甲中阴极增重0.27 g,乙中阴极增重0.14 g,则元素G的相对原子质量为(?? )
 ?????????????
?????????????
A.112
B.73
C.64
D.65
2、填空题 (16分)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,
总反应为:2CH3CHO + H2O ="==" CH3CH2OH + CH3COOH。实验室中,以一定浓度的乙醛―Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。

(1)若以甲醇燃料电池为该电解的直流电源,燃料电池中的电解液是氢氧化钠溶液,则燃料电池中b极的电极反应式为 。电池工作一段时间后,氢氧化钠溶液物质的量浓度 (填变大,变小或不变)
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。阳极电极反应如下:① 4OH- - 4e-="=" O2↑+ 2H2O;②
(3)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
(4)若直流电源使用新型的熔融碳酸盐燃料电池(MCFS),该电池以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650 ℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1∶1)直接作燃料,其工作原理如图所示。
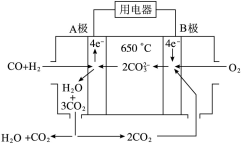
①B极发生______(填“氧化”或“还原”)反应,电极反应式 。
②以此电池电解足量的CuSO4溶液,当电池消耗1.12L(标准状况下)氧气时,则阴极产物的质量为_ _____ g。加入一定量的 可以让CuSO4溶液回复原状。
A、CuO B、Cu(OH)2 C、CuCO3 D、Cu
3、选择题 应用电解法制备的物质主要有三种:一是铝的工业制备;二是电解饱和NaCl溶液制备烧碱;三是金属钠的制备.下列关于这三个工业生产的描述中正确的是( )
A.电解法制铝时一般是用熔融态的氧化铝进行电解,但也可用熔融态的A1C13
B.电解法生产铝时,每转移3mol电子的时候,就能生产出1mol的铝
C.在电解饱和NaCl溶液中,电解池中的阴极产生的是H2,NaOH在阳极附近产生
D.电解饱和NaCl溶液和金属钠的冶炼都用到了NaC1,在电解时它们的阴极都是C1-失电子
4、选择题 LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4。电池的正极材料是LiFePO4,负极材料是石墨,含有导电固体为电解质。下列有关LiFePO4电池的说法不正确的是 [???? ] LiFePO4。电池的正极材料是LiFePO4,负极材料是石墨,含有导电固体为电解质。下列有关LiFePO4电池的说法不正确的是 [???? ]
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+向正极移动
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4
5、填空题 (8分)氯碱工业中电解饱和食盐水的原理示意图如下图所示:

(1)电极a是电源的??????。
(2)溶液A的溶质是(填化学式)????????????????。
(3)电解饱和食盐水的离子方程式是??????????????????????????????。
(4)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用???? _______________________________________________________?????????。
(5)电解所用的盐水需精制,去除盐水中的Ca2+、Mg2+、NH4+和SO42-,提供的试剂有① Na2CO3溶液② BaCl2 溶液③ NaOH溶液④ HCl,加入试剂的顺序是________________。
|