��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��8�֣�����ͼ��ʾ��������ַ�Ӧ��
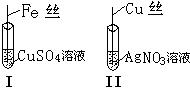
�� I����˿�Ϲ۲쵽������ ��??????????????????????????
��?????????????????????????? ???????��
???????��
��Ӧ�Ļ�ѧ����ʽΪ??????????????????????????��
�� II�з�����Ӧ�Ļ�ѧ����ʽΪ ???????????????????????��
???????????????????????��
�ǽ��I��IIʵ�������֪��Fe��Cu��Ag�Ļ�ԭ��˳��Ϊ??????????????????��
�ο��𰸣���8�֣�
��1����˿�ϸ���һ���ɫ���壻Fe+CuSO
�����������
�����Ѷȣ�һ��
2��ѡ���� ��������I��II����ȷ�����������ϵ����
ѡ��
| ����I
| ����II
|
A
| NH4ClΪǿ��������
| �ü��ȷ���ȥNaCl�е�NH4Cl
|
B
| Fe3+����������
| ��KSCN��Һ���Լ���Fe3+
|
C
| �ܽ�ȣ�CaCO3<Ca(HCO3)2
| �ܽ�ȣ�Na2CO3<NaHCO3
|
D
| SiO2����HF��Ӧ
| �����ܱ����ڲ���ƿ��
�ο��𰸣�D
���������NH4ClΪǿ�������ε�ԭ����HCl��ǿ�ᡢNH3?H2O������ü��ȷ���ȥNaCl�е�NH4Cl��ԭ����NH4Cl�����ֽ�Ϊ�������Ȼ������壬��NaCl�����ȶ��Ժ�ǿ�������I��II����ȷ����������û�������ϵ��A�����Fe3+���������Ե�ԭ������Ԫ�صĻ��ϼۿ��Դ�+3�۽�Ϊ+2������0�ۣ���KSCN��Һ���Լ���Fe3+��ԭ����Fe3+��KSCN��ҺѸ���Ժ�ɫ�������I��II����ȷ����������û�������ϵ��B�������̼�������Һ��ͨ�����������̼����ɵó�����Һ��˵��̼�����������ˮ�ĸ��Σ�̼����
�����Ѷȣ�һ��
3������� ��֪ij��Ͻ�����ĩ�У��������������ͭ�е�һ�ֻ����֣�����������������5%���ϡ�����ƺ���ʵ��̽���û���������ĩ������ͭԪ�صĴ��ڡ�
 ����ѡ����������Լ����ձ����Թܡ�����������Ͳ������ƿ���ιܡ�ҩ�ף�1mol��L-1���ᡢ2mol��L-2���ᡢ2mol��NaOH��Һ��20%KSCN��Һ�� ����ѡ����������Լ����ձ����Թܡ�����������Ͳ������ƿ���ιܡ�ҩ�ף�1mol��L-1���ᡢ2mol��L-2���ᡢ2mol��NaOH��Һ��20%KSCN��Һ��
 �������ʵ��̽�����̣� �������ʵ��̽�����̣�
 ��1��������裺 ��1��������裺
 ����1���û�Ͻ�����ĩ�г��������?????Ԫ�أ� ����1���û�Ͻ�����ĩ�г��������?????Ԫ�أ�
 ����2���û�Ͻ�����ĩ�г��������?????Ԫ�أ� ����2���û�Ͻ�����ĩ�г��������?????Ԫ�أ�
 ����3���û�Ͻ�����ĩ�г��������Fe��CuԪ�أ� ����3���û�Ͻ�����ĩ�г��������Fe��CuԪ�أ�
 ��2�����ʵ�鷽�����ڼ���3����Ƴ�ʵ�鷽������Ҫ�ڴ�������𣩡� ��2�����ʵ�鷽�����ڼ���3����Ƴ�ʵ�鷽������Ҫ�ڴ�������𣩡�
 ��3��ʵ����� ��3��ʵ�����
 ���ݣ�2����ʵ�鷽��������ʵ�������Ԥ������ͽ��ۡ� ���ݣ�2����ʵ�鷽��������ʵ�������Ԥ������ͽ��ۡ�
 ����ʾ�����ڴ���ϰ����·�ʽ����ע��ǰ�����ݶ�Ӧ�� ����ʾ�����ڴ���ϰ����·�ʽ����ע��ǰ�����ݶ�Ӧ��
 ��ע�����ּ�࣬ȷ������������ռ䡣 ��ע�����ּ�࣬ȷ������������ռ䡣
�ο��𰸣���1��Cu��Fe��˳��ɽ����� ��������� ��������� ����ѧ����Ԫ�ػ��������ʵ����գ�����ѧ�������ʽ��м����ʵ�鼼�ܺͶ�ʵ���� ����ѧ����Ԫ�ػ��������ʵ����գ�����ѧ�������ʽ��м����ʵ�鼼�ܺͶ�ʵ����
 ������������Ҫ��;��ʹ�÷������� ������������Ҫ��;��ʹ�÷�������
�����Ѷȣ�һ��
4��������
(1)������a g Cu�ۣ��ڼ��������£��������ַ�Ӧ��Ȼ�����ɵ�CuOȫ������������ϡHNO3��Һ�У��Ƶ�Cu(NO3)2��Һ�������ĵ�O2�����ʵ�����??????????????��
���ĵ�HNO3�����ʵ�����???????????????????????????
(2)������a g Cu��ȫ������һ������ŨHNO3�У�������ɵ������ڱ�״�������Ϊb L
(������NO2ת����N2O4)�������ĵ�HNO3�����ʵ�����???????mol��
Ϊ������Ⱦ�������ɵ�����ͨ��ˮ�в�ͬʱͨ��O2��ʹ���ɵ�������ȫ����ˮ��������O2�����ʵ�����???????mol���������ɵ�����ͨ��NaOH��Һ�У����屻��ȫ���գ�����ֻ��NaNO3��NaNO2��H2O��������NaNO2�����ʵ�����??????????????mol��
�ο��𰸣�
 ������������⿼������غ��Ԫ���غ㣬���е��Ѷȡ�(1)n(O2)=ag/[64g��mol-1��2]= a/128mol ������������⿼������غ��Ԫ���غ㣬���е��Ѷȡ�(1)n(O2)=ag/[64g��mol-1��2]= a/128mol
n(HNO3)="2" n(Cu)= 2ag/64g��mol-1��a/32mol ��(2)���õ�Ԫ���غ㣬�ɵ����ĵ�HNO3�����ʵ�����a/32 +b/22.4��mol��������a g Cuʧȥ�ĵ�������O2�õ��ĵ�������ȣ��ɵ�����O2�����ʵ�����n(O2)=a/128mol����ֱ��ͨ��NaOH��Һ�����屻��ȫ���գ�����ֻ��NaNO3��NaNO2��H2O��������NaNO2�����ʵ��������õ�
�����Ѷȣ�һ��
5������� ��1�����к�Fe2O380%�ij�����100t�������Ͽ�ұ����Fe95%���������ٶ֣�
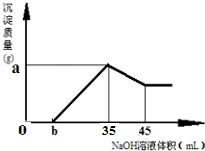
��2��ȷ��ȡ6g������Fe2O3��Al2O3����Ʒ������ʢ��100mLHCl���ձ��У���ַ�Ӧ����ˣ�����Һ�м���10mol?L-1��NaOH��Һ�������ij�������������NaOH��Һ������Ĺ�ϵ��ͼ��ʾ������
����������ʵ���Ũ���Ƕ��٣�
����b=2.3�����������������������������Ƕ��٣�
�ο��𰸣���1������Ŀ��֪��m�� Fe2O3���T100t��80%�T80
���������
�����Ѷȣ�һ��
|