微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 可逆反应2NO2(g)?2NO(g)+O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n?molO2的同时生成2n?mol NO2
②单位时间内生成n?molO2的同时生成2n?mol NO
③NO2、NO、O2的物质的量浓度比值为2:2:1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的总压强不再改变的状态.
A.①④⑥
B.②③⑤
C.①③④
D.全部
参考答案:①根据单位时间内生成n molO2的同时生成2n mol N
本题解析:
本题难度:简单
2、选择题 在一个不传热的固定容积的密闭容器中,可逆反应N2(气)+3H2?(气)

2NH3(气)+Q达到平衡的标志是( )
a.反应速率υ(N2):υ(H2):υ(NH3)=1:3:2;
b.各组分的物质的量浓度不再改变;
c.体系的压强不再发生变化;
d.混合气体的密度不变(相同状况);
e.体系的温度不再发生变化;
f.2υ(N2)?(正反应)=υ(NH3)(逆反应);
g.单位时间内?3mol?H-H键断裂的同时有6mol?N-H键断裂.
A.abcef
B.bcdef
C.bcefg
D.bcdfg
参考答案:a.无论是否达到平衡状态,化学反应速率之比都等于化学计量数之
本题解析:
本题难度:一般
3、计算题 一氧化碳变换反应 CO(g)+ H2O(g)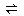 ?H2(g)+ CO2(g),在773K时,平衡常数Kc =" 9" ,如反应开始时CO和H2O的浓度都是0.020 mol/L ,计算在次条件下,CO的最大转化率是多少?
?H2(g)+ CO2(g),在773K时,平衡常数Kc =" 9" ,如反应开始时CO和H2O的浓度都是0.020 mol/L ,计算在次条件下,CO的最大转化率是多少?
参考答案:一氧化碳最大的转化率是75% 。
本题解析:CO(g) +??? H2O(g)?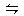 ???CO2(g)? +?? H2(g)
???CO2(g)? +?? H2(g)
初始浓度/mol・L-1:0.020???????? 0.020????????????? 0???????????? 0
转化浓度/mol・L-1: x???????????? x??????????????? x??
本题难度:一般
4、选择题 在盛有足量 A 的体积可变的密闭容器中,加入B ,发生反应:

A (s)+2B(g) 4C(g) + D ( g );△H < 0 。
4C(g) + D ( g );△H < 0 。
在t℃.p KPa下达到平衡。平衡时 C 的物质的量与加入的 B
的物质的量的变化关系如右图。下列说法正确的是??(???)
A.平衡 时B的转化率为33.3 %
时B的转化率为33.3 %
B.若再加入B,则再次达到平衡时正.逆反应速率均增大,但仍然相等
C.若再加人4molC和1molD ,则再次达到平衡时体系气体密度减小,平均摩尔质量不变
D.若温度变为(t+10)℃,则θ<45°
参考答案:D
本题解析:略
本题难度:简单
5、填空题 以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应: 2CO2(g)+6H2(g)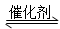 CH3CH2OH(g)+3H2O(g) -Q(Q>0)
CH3CH2OH(g)+3H2O(g) -Q(Q>0)
在密闭容器中,按H2与CO2的物质的量之比为3:1进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。
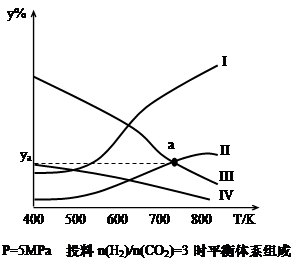
完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是_______(选填序号)
(2)在一定温度下反应达到平衡的标志是_______(选填编号)
a.平衡常数K不再增大
b.CO2的转化率不再增大
c.混合气体的平均相对分子质量不再改变
d.反应物不再转化为生成物
(3)其他条件恒定,如果想提高CO2的反应速率,可以采取的反应条件是_______(选填编号);达到平衡后,能提高H2转化率的操作是_______(选填编号)
a.降低温度???? b.充入更多的H2?
c.移去乙醇?? d.增大容器体积
(4)图中曲线II和III的交点a对应的体积分数ya=_______%
参考答案:(1)II(2分)
(2)bc(2分)?
(3)
本题解析:
试题分析:(1)反应过程中反应物逐渐减少,生成物逐渐增多,变化量的关系符合化学计量数比值,故Ⅰ、Ⅱ、Ⅲ、Ⅳ分别为H2O、CH3CH2OH、H2、CO2(g) ;
(2)遵循“变量不变达平衡”,a、温度不变平衡常数不变,错误;b、转化率从0到最大,是变量,不变时达到平衡,正确;c、气体的质量不变,容器的体积不变,混合气体的密度是定值,错误;d、平衡是动态平衡,每种物质的生成速率和消耗速率相等,错误;
(3)提高反应物的转化率可以改变温度使平衡正向移动,或增加另一种反应物的浓度,或移去产物
本题难度:一般