��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��Ӧ4NH3��g��+5O2��g��=4NO��g��+6H2O��g����1.0L�ܱ������н��У�����Ӻ�ˮ���������ʵ���������4.5mol����˷�Ӧ��ƽ������v��x������Ӧ����������ʻ������������ʣ��ɱ�ʾΪ�� ? ��
A��v��NH3��=0.010mol/��L?s��
B��v��O2��=0.10mo1/��L?s��
C��v��NO��=0.10mo1/��L?s��
D��v��H2O��=0.45mol/��L?s��
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� ������ʵ��������������ԭ�����͵���(? )
A������ѹǿ�������ڶ��������������Ӧ������������
B����ҵ��ȡ����ͺϳɰ���Ӧ��Ҫʹ�ô���
C���ϳɰ���ҵ�����У��Ѻϳ����еİ������ϳ��
D��ʵ���ҳ����ű���ʳ��ˮ�ķ����ռ�����
�ο��𰸣�B
���������
����������������������������������ķ�Ӧ�����������С�ķ�Ӧ������ѹǿ��ƽ����������������ķ����ƶ���A��ȷ������ͬ�ȳ̶ȸı������淴Ӧ���ʣ���ƽ���ƶ���Ӱ�죬B��������ɳ����ԭ�����ͣ��ϳɰ���Ӧ�У��Ѱ��Ƴ�������������Ũ�ȣ�ƽ�������ƶ���C��ȷ����������ˮ�ķ�Ӧ��Cl2+H2O H++Cl-+HClO���ǿ��淴Ӧ������ʳ��ˮ��������Ũ�ȴ�����������Ũ�ȣ�ƽ�������ƶ���D��ȷ��
H++Cl-+HClO���ǿ��淴Ӧ������ʳ��ˮ��������Ũ�ȴ�����������Ũ�ȣ�ƽ�������ƶ���D��ȷ��
����������ͬ�ȳ̶ȸı������淴Ӧ���ʣ���ƽ���ƶ���Ӱ�졣
�����Ѷȣ�һ��
3��ѡ���� ����mA(g)+nB(g)  p C(g)+qD(g)��ͼ��Y���ʾƽ����ϵ��C�İٷֺ�����C%��������˵������ȷ���ǣ���?��
p C(g)+qD(g)��ͼ��Y���ʾƽ����ϵ��C�İٷֺ�����C%��������˵������ȷ���ǣ���?��

A��Y��ɱ�ʾ�������ƽ��Ħ������
B��m+n��p+q
C������Ӧ����
D��Y��ɱ�ʾ����A��ת����
�ο��𰸣�CD
�����������ͼ���ã�ѹǿ����ƽ����ϵ��C�İٷֺ������٣�����ƽ�������ƶ�������m+n��p+q����B����
��������ƽ��Ħ������=��������������/�������������ʵ�������ΪA��B��C��D���߾�Ϊ���壬�������غ㣬�ã���������������Ϊһ��ֵ����Ϊm+n��p+q�����ԣ�ѹǿ����ƽ�������ƶ�ʱ���������������ʵ�����С�����������ƽ��Ħ������Ӧ�����������ߵ��½����ƣ���A����
ͬ����ѹǿ����ƽ�������ƶ�ʱ������A��ת����Ӧ��С����D��ȷ��
����ͼ�е����ߣ���ʾ��ͬһѹǿ�£����£�ƽ����ϵ��C�İٷֺ���������ƽ�������ƶ������ԣ�����Ӧ���ȣ���C��ȷ��
�����Ѷȣ�һ��
4������� ij�¶�ʱ����2L�ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ���
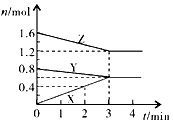
��1���÷�Ӧ�Ļ�ѧ����ʽ��_____________________��
��2����Ӧ��ʼ��2minĩ��X�ķ�Ӧ����Ϊ______________��mol��L-1��min-1����
��3��3min��ͼ����������ʾ�ĺ�����______________________��
�ο��𰸣���1��Y+2Z![]() ���������
���������
�����Ѷȣ�һ��
5��ѡ���� ��2A��B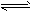 3C��4D�У���ʾ�÷�Ӧ����������
3C��4D�У���ʾ�÷�Ӧ����������
[???? ]
A����(A) = 0��5mol��L-1��S-1
B����(B) = 0��3 mol��L-1��S-1
C����(C) = 0��8mol��L-1��S-1
D����(D)= 1 mol��L-1��S-1
�ο��𰸣�B
���������
�����Ѷȣ���