微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将等物质的量的F2和ClF混合,在密闭容器中发生反应: F2(g)+ClF(g)  ClF3(g);△H<0。下列叙述中,正确的是
ClF3(g);△H<0。下列叙述中,正确的是
A.恒温恒容时,当ClF 转化40% 时,容器内的压强为初始时的0.6 倍
B.若 c(F2):c (ClF): c (ClF3) ="1:" 1: 1,则反应一定达到平衡状态
C.达到平衡后,若增大容器容积,则正反应速率减小,逆反应速率增大,平衡左移
D.平衡后再降低温度,保持恒容,达到新的平衡,则混合气体的平均摩尔质量增大
参考答案:D
本题解析:A :采用“三段式”可得出,平衡时混合气体的总物质的量为1.6 mol,压强为初始时的0.8倍
B:c(F2):c (ClF): c (ClF3) ="1:" 1: 1与是否平衡没有直接关系
C:若增大容器容积,各物质浓度均减小,正逆反应速率均减小
D:降温,平衡正向移动,气体总物质的量减小,平衡摩尔质量增大,正确
故答案为D
本题难度:一般
2、选择题 工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2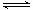 2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
A.使用催化剂是为了加快反应速率,提高生产效率
B.在上述条件下,SO2不可能100%地转化为SO3
C.达到平衡时,改变反应条件可能在一定程度上改变该反应的化学平衡状态
D.达到平衡时,SO2的浓度与SO3的浓度一定相等
参考答案:D
本题解析:
试题分析:使用催化剂是为了加快反应速率,提高生产效率,A正确;该反应是可逆反应,所以在上述条件下,SO2不可能100%地转化为SO3,B正确;平衡状态是一定条件下的,如果改变外界条件,平衡状态可以发生变化,C正确;在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此选项D不正确,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。侧重考查学生对可逆反应平衡状态特点以及外界条件对平衡状态影响的熟悉了解程度,有利于调动学生的学习兴趣,提高学生的学习效率和应试能力。
本题难度:一般
3、选择题 下列措施或事实不能用勒沙特列原理解释的是(????)
A.滴加酚酞的氨水中加入氯化铵固体后红色变浅
B.棕红色的NO2加压后颜色先变深后变浅(已知: 2NO2 (g) 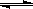 N2O4 (g))
N2O4 (g))
C.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率
D.煅烧粉碎的硫铁矿利于SO2的生成
参考答案:D
本题解析:如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,中这就是勒夏特列原理,该原理适用于所有的平衡体系,因此选项A、B、C都可以用勒夏特列原理解释。选项D中的反应是燃烧,不是可逆反应,不能用勒夏特列原理解释,答案选D。
本题难度:一般
4、选择题 一定条件下,下列不能用勒夏特列原理解释的是?
A.工业生产硫酸的过程中使用适当过量氧气,以提高SO2的转化率
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后气体颜色变深
C.实验室用排饱和NaHCO3溶液的方法收集CO2气体
D.新制氯水中,滴加硝酸银溶液,溶液颜色变浅,产生白色沉淀
参考答案:B
本题解析:A中增大氧气的浓度,平衡向正反应方向移动,提高SO2的转化率。氢气和碘蒸汽生成碘化氢的反应是体积不变的可逆反应,增大压强,浓度变大,颜色加深,但平衡不移动,不能用勒夏特列原理解释。C属于溶解平衡,正确。D属于沉淀溶解平衡,正确,所以答案是B。
本题难度:简单
5、填空题 合成氨是重要的化学工业,为了研究合成氨的反应原理,在一密闭容器内充入1 mol N2和2 mol H2,在一定条件下,使之发生如下反应:N2+3H2?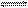 ??2NH3。
??2NH3。
Ⅰ:若维持温度不变,且密闭容器的容积固定为1 L。
L。
(1) 当此反应经过2 min达到平衡状态时,测得反应混合物中NH3的物质的量为0.2 moL,则H2在2 min内的平均反应速率为__________________。
(2)如果开始时,向该容器内加入0.5 moL N2,要使反应混合物中三种气体的物质的量分数仍与上述平衡时的完全相同,则还必须加入H2 _______mo l和NH3 _______mol。
l和NH3 _______mol。
(3)如果开始时加入N2、H2、NH3的物质的量分别为a mol 、b mol 、c mol ,要使反应达到平衡状态时,反应混合物中三种气体的物质的量分数仍与(1)平衡时完全相同,则a、b、c应满足的一般条件是(a、b分别用含c的方程式表示)?????????????????。
Ⅱ:若温度维持不变,体系压强维持与Ⅰ相同,密闭容器的容积由1 L随反应进行而改变。
(4)开始时加入1 mol N2和2 mol H2,经过一段时间,容器中三种气体的物质的量分数不再发生变化时,则NH3的物质的量为__________(选填一个编号)
(甲)大于0.2 mol???? (乙)等于0.2 mol
(丙)小于0.2 mol ????(丁)可能大于、等于或小于0.2mol
作出此判断的理由是__________________________________________。
参考答案:
(1)0.15 mol・L-1・min-1 (2分)
本题解析:略
本题难度:一般