微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于晶体的说法一定正确的是
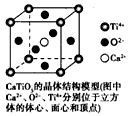 [???? ]
[???? ]
A.分子晶体中都存在共价键
B.CaTiO3品体中每个Ti4+与12个O2-相紧邻
C.SiO2晶体中每个硅原子与2个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
2、填空题 (5分)(1)下列数据是对应物质的熔点(℃)
NaCl
| Na2O
| AlF3
| AlCl3
| BCl3
| Al2O3
| CO2
| SiO2
|
801
| 920
| 1291
| 190
| -109
| 2073
| -57
| 1723
据此作出的下列判断中,错误的是
A.铝的化合物晶体中没有离子晶体
B.表中只有BCl3,干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si和Si―O键的比例为??????????。
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。
化学键
| Si―O
| Si―Si
| O=O
| 键能kJ/mol
| 460
| 176
| 498
Si(s)+O2(g) SiO2(s),该反应的反应热△H=?????????。 SiO2(s),该反应的反应热△H=?????????。
3、选择题 下图所示为某晶体的一个晶胞,该晶体由A、B、C三种基本粒子组成。试根据晶胞判断,该晶体的化学式为
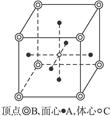
A.A6B8C???????????? B.A2B4C??????????? C.A3BC???????????????? D.A3B4C
4、选择题 下列说法中正确的是[???? ]
A. SO2和O3、PO43-和ClO4-互为等电子体
B. 甲烷分子失去一个H+,形成CH3-,其碳原子的杂化类型发生了改变
C. Ti原子的核外电子排布式为[Ar]3d34s2
D. CS2、H2O、C2H2都是直线形分子
E. CH4、BCl3、CO2都是含有极性键的非极性分子
5、选择题 在x mol石英晶体中,含有Si-O键数是
A.x mol
B.2x mol
C.3 x mol
D.4x mol
|
|