微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (10分)实验室制取乙酸乙酯的主要步骤如下:
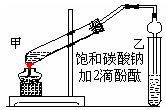
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液.
②按右图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层。④分离出乙酸乙酯层、洗涤、干燥。
(1)反应中浓硫酸的作用是___________________写出制取乙酸乙酯的化学方程式:___________________________________;
(2)上述实验中饱和碳酸钠溶液的作用是(填字母):_______________。
A.中和乙酸和乙醇。
B.中和乙酸并吸收部分乙醇。
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出。
D.加速酯的生成,提高其产率。
(3)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有???__________;分离时,乙酸乙酯应该从仪器?? ________??????(填:“下口放” 或“上口倒”)出。
参考答案:(1)催化剂,吸水剂(2分)???? CH3COOH+CH3
本题解析:考查乙酸乙酯的制备。
(1)在酯化反应中浓硫酸作催化剂,又因为酯化反应是可逆反应,所以浓硫酸还起吸水剂的作用。乙醇和乙酸除生成乙酸乙酯外,还有水生成。
(2)由于乙醇和乙酸易挥发,在生成的乙酸乙酯中混有乙醇和乙酸。所以利用饱和碳酸钠溶液可以中和乙酸并吸收部分乙醇,同时乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出。因此答案是BC。
(3)乙酸乙酯难溶于水,且密度小于水的。所以通过分液漏斗进行分离,其中乙酸乙酯从分液漏斗的上口倒出。
本题难度:一般
2、选择题 在配制100mL 2mol/L的NaOH溶液时,下列操作会导致结果偏低的是(?? )
(1)用拖盘天平称量时砝码放在左盘
(2)溶解NaOH固体后没有冷却至室温就向容量瓶转移溶液
(3)将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
(4)定容时俯视刻度线
(5)定容时仰视刻度线
(6)干净的容量瓶未经干燥就用于配制溶液
A.(2)(4)(6)
B.(1)(3)(4)
C.(1)(3)(5)
D.(2)(3)(4)
参考答案:C
本题解析:略
本题难度:简单
3、实验题 (10分,每空2分)
漂白粉可以和浓盐酸反应产生氯气,某课外兴趣小组试图测定氯气的体积并验证纯净干燥的氯气没有漂白性,现用如图所示装置进行实验,请回答有关问题:

(1)该装置的正确连接顺序是:a接(??? )、(??? )接(??? )、(??? )接(??? )、(??? )接(??? )、(??? )接(??? )。
(2)U型管可以用内盛装__________的洗气瓶代替
(3)在制取氯气前,必须进行的一项操作步骤是__________________
(4)按照实验目的进行之后,干燥有色布条是否褪色(??? )(填是或否)。
(5)该兴趣小组在实验中,发现量筒中并没有收集到液体,你认为他们失败的原因可能是____________________________________________________。
参考答案:(1)a接(d)、(e)接(b或c)、(c或b)接(g)、(
本题解析:
试题分析:(1)实验装置的连接顺序,遵循“发生装置―除杂装置―性质检验装置―气体收集装置―尾气处理装置”,故其连接顺序为:a接(d)、(e)接(b或c)、(c或b)接(g)、(h)接(e)、(d)接(f)。
(2)U型管中的无水CaCl2的作用主要是吸收水蒸气,因此可用盛装浓硫酸的洗气瓶代替。
(3)对于有气体生成的装置,实验进行前都应对装置的气密性进行检查。
(4)干燥的氯气不能使干燥的有色布条褪色,因为使有色布条褪色的为具有强氧化性的HClO。
(5)对于气体的收集,若反应后无法收集到气体,可从装置的气密性、反应的发生进行考虑。
点评:本题考查了氯气的制备和性质实验,结合了实验装置综合考查了实验的连接以及实验装置的作用,是一道非常有价值的题目。既考查了学生的基础知识,又综合考查了学生的动手实验能力。
本题难度:一般
4、填空题 下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是
A.SO2、H2S、Cl2
B.SO2、O2、NH3
C.SO2、CO2、O2
D.HCl、H2S、HI
参考答案:C
本题解析:A中三者不能共存(因:SO2+2H2S=3S+2H2O H2S+Cl2=S+2HCl),且H2S不能用浓硫酸干燥(因H2S具还原性,浓硫酸有强氧化性,所以H2S能被浓硫酸氧化);
B中SO2、NH3不能共存(因两者能发生反应),NH3不能用浓硫酸干燥(因2NH3+H2SO4=(NH4)2SO4);
D中三者能共存,但H2S、HI不能用浓硫酸干燥(原因同A,发生氧化还原反应);
本题难度:一般
5、实验题 (本题共12分)
氯气和氯乙烯都是重要的化工产品,年产量均在107t左右。氯气的实验室制备和氯乙烯的工业生产都有多种不同方法。
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要_________、________(填写试剂或溶液名称)
(2)实验室用2.00mol/L的盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为_________m,l。
(3)实验室通常用向上排空气法收集氯气。设计一个简单实验,验证所收集的氯气中是否含有空气。
_________________
4)工业上用电石-乙炔法生产乙烯的反应如下:
CaO+3C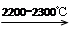 CaC2+CO
CaC2+CO
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH↑+HCl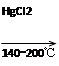 CH2=CHCl
CH2=CHCl
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。
电石-乙炔法的缺点是___________________、_____________________。
(5)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件)。
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。
___________________________________
参考答案:(1)饱和氯化钠溶液、氢氧化钠溶液?? (2)100
本题解析:
试题分析:(1)浓盐酸易挥发,生成的氯气中含有氯化氢,应该用饱和氯化钠溶液除去;氯气有毒需要尾气处理,用氢氧化钠溶液吸收。
(2)根据反应物和生成物可知,反应的化学方程式为4HCl+Ca(ClO)2→CaCl2+2H2O+2Cl2↑,反应中生成氯气的物质的量是0.1mol,则消耗氯化氢的物质的量是0.2mol,盐酸的浓度是2.00mol/L,因此需要盐酸的溶液的体积是100ml。
(3)氯气能与氢氧化钠溶液完全反应,而空气与氢氧化钠不反应,据此检验,即试管收集氯气,收集满后讲试管倒立在氢氧化钠溶液中,观察试管内有无残留气体。
(4)根据流程可知,反应需要高温,因此缺点之一是高能耗;需要氯化汞作催化剂,汞是重金属,因此缺点之二是会污染环境。
(5)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢,产生的氯化氢可以与乙炔反应又生成氯乙烯,因此方案为CH2=CH2+Cl2→ClCH2CH2Cl、ClCH2CH2Cl→CH2=CHCl+HCl、HC≡CH+HCl→CH2=CHCl。
本题难度:一般