��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��ʽ̼��ͭ��һ�ֻ���ԭ�ϣ���ѧʽ��mCu(OH)2��nCuCO3��ʾ��ʵ�����Է�ͭмΪԭ����ȡ��ʽ̼��ͭ�IJ������£�
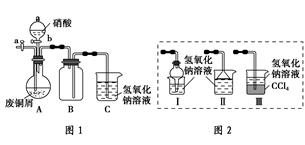
��.��ͭм������ͭ
����1����ͭм�ڿ����г�����գ�������������ϡ���
����2����ͼ1(�г�������ʡ��)����Ũ���Ỻ���ӵ���ͭм��(��ͭм����)����ַ�Ӧ����ˣ��õ�����ͭ��Һ��
����3��������2��Ũ���ỻ��ϡ���ᣬ�������䡣
��.��ʽ̼��ͭ���Ʊ�
������Թ��м���̼������Һ������ͭ��Һ
��ˮԡ������70 ������
����0.4 mol��L��1��NaOH��Һ����pH��8.5�������á�����
������ˮϴ�ӡ���ɣ��õ���ʽ̼��ͭ��Ʒ
��ش��������⣺
(1)������1ʵ�飬����ѡ�������������________(�����)��
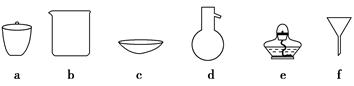
(2)ͼ2���ֱܷ����ͼ1��B��Cװ�õ���________(��װ�����)��
(3)��֪��NO��NO2��2NaOH===2NaNO2��H2O��2NO2��2NaOH===NaNO3��NaNO2��H2O��NO���ܵ�����NaOH��Һ��Ӧ��ʵ�����ʱ����β�������ʹװ���е��ж����屻NaOH��Һ��ȫ���գ�__________________________��
(4)�������ϴ�ӵ�Ŀ����______________________________________��
(5)����۹��˺����Һ�к���CO32��������CO32���ķ�����_________________________________________________________��
(6)�ⶨ��ʽ̼��ͭ��ɵķ�����Ҫ�����֣�
����1�����շ���ȡ34.6 g������mCu(OH)2��nCuCO3����Ӳ���Թ������գ��������������ͨ��������Ũ���ᡢ�����ļ�ʯ���У���ȫ���պ�Ũ���Ά��1.8 g����ʯ�Ҿ���8.8 g��
����2����ԭ�����������м�ǿ�ȣ��ⷴӦǰ������������
�������������������ʽ̼��ͭ�Ļ�ѧʽ_____________________��
����ƽ��ѧ����ʽ��mCu(OH)2��nCuCO3��________H2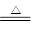 ________Cu��________CO2����________H2O
________Cu��________CO2����________H2O
2�������� ��5�֣�ʵ������8.7g��MnO2��������Ũ������ȡ�������������������������״�����ͱ�������HCl�����ʵ�����
3������� ��10�֣�����ͼʾװ����ȡ������������������գ�

��1��Ϊ��ֹa�е�Һ����ʵ��ʱ�������У��ڼ���ǰӦ��ȡ
�Ĵ�ʩ��??????????????????���Թ�b�м���????????????????
��Һ����������???????????????????????????????��
��2��ʵ���м����Թ�a��Ŀ���ǣ�
��?????????????????????????????????????????????��
��?????????????????????????????????????????????��
��3��ͼ��һ�����ԵĴ�����?????????????????????��
4��ʵ���� ��16�֣���ȸʯ��Ҫ��Cu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4��5H2O��CaCO3���������£�

�Իش��������⣺
��1����δ����H2O2����ҺA�У����ڵĽ���������Cu2+��Fe2+��Fe3+�����������Һ��Fe3+��ѡ������ʵ��Լ���?����?������ţ���
A��KMnO4��Һ
B��Fe��
C��Na2CO3��Һ
D��KSCN��Һ
����ҺA�м���H2O2��H2O2�ڸ÷�Ӧ������������ʵ����ѡ��H2O2������Cl2���������������ǻ��������⣬��һԭ���Dz��������������������ӡ�
��2������ҺC���CuSO4��5H2O����Ҫ��������Ũ����???�����������˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������������������
��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��?������������������������������?����ʵ��������а����ݳ�����ѡ������װ���е�?����?������ţ�װ�����հ�����
���ձ��е�Һ�嶼Ϊˮ��
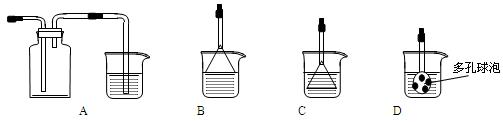
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100 mL 0.1 mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������??����������???�������ò��������м�����ˮ���ӽ��̶���1��2cmʱ��Ӧ�������������������μ�����ˮ����Һ�İ�Һ��������̶�����ƽ��
5��ѡ���� ���Ⱦ۱�ϩ�����Ͽ��Եõ�̼�����������顢��ϩ����ϩ�����ͼױ�����ͼ��ʾװ��̽���Ͼ����ϵ������á�������������ȷ����(????? )
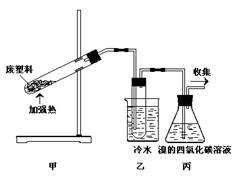
A���۱�ϩ�������ǡ�CH2��CH2��CH2��
B��װ���ҵ��Թ��п��ռ���������
C��װ�ñ��е��Լ�������ϩ������ȡ±����
D������ռ����������ȼ��