微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铝的以下反应得以进行的原因,可用勒沙特勒原理解释的是
A.与盐酸反应产生氢气
B.在氯气中燃烧
C.放入硝酸汞溶液中表面形成铝汞齐
D.一定温度下,用铝与氧化钙反应制得金属钙
参考答案:D
本题解析:
试题分析:ABC都是进行很快的反应,不可逆,不可解释,错误;D.一定温度下,用铝与氧化钙反应制得金属钙,有利于平衡向生成钙的正反应方向移动,正确。
本题难度:一般
2、选择题 一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)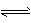 H2(g) +I2(g)。若c(HI)由 0.1 mol.L-1降到0. 07 mol.L-1时,需要15 s,那么c(HI)由 0.07 mol.L-1降到0.05 mol.L-1时,所用的时间为
H2(g) +I2(g)。若c(HI)由 0.1 mol.L-1降到0. 07 mol.L-1时,需要15 s,那么c(HI)由 0.07 mol.L-1降到0.05 mol.L-1时,所用的时间为
[???? ]
A.等于5s
B.等于10 s
C.大于10 s
D.小于10 s
参考答案:C
本题解析:
本题难度:一般
3、填空题 在一密闭的2 L容器中装有4 mol SO2和2 mol O2,在一定条件下开始反应。2 min末测得容器中有1.6 mol SO2,请计算:(1)2 min末SO3的浓度???????;(2)2 min内SO2的平均反应速率?????????(3)2 min末SO2与O2的压强的比???????。
参考答案:(第(1)题3分,其余每空2分)1.2 mol/L;? 0.
本题解析:
试题分析:该反应的化学方程式是
2SO2????+??? O2 2SO3
2SO3
起始浓度(mol/L)?? 2?????????? 1?????? 0
转化浓度(mol/L)?? 1.2???????? 0.6???? 1.2
2min末浓度(mol/L) 0.8??????? 0.4????? 1.2
所以2 min末SO3的浓度是1.2mol/L
2 min内SO2的平均反应速率是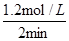 =0.6 mol/(L・min)
=0.6 mol/(L・min)
在温度和体积相同的条件下,气体的压强之比是物质的量之比
所以2 min末SO2与O2的压强的比1.2:0.6=2:1
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某时刻的量,然后依据已知条件列式计算即可,有利于培养学生的规范答题能力。
本题难度:一般
4、选择题 已知某指定反应物(A)的平衡转化率(α)的数学表达式可用下式表示:

下列各项叙述中,表明平衡肯定发生移动的是??????????????????(???)
A、反应混合物的浓度改变?????????? B、反应混合物的压强改变
C、正、逆反应速率改变???????????? D、反应物的转化率改变
参考答案:D
本题解析:只要反应过程中正反应速率和逆反应速率不相等,则平衡就一定发生移动。根据转化率的概念可知,如果转化率发生变化,则平衡一定发生了变化,D正确。ABC都是不一定的,答案选D。
本题难度:一般
5、选择题 在一定温度下A(气)+3B(气)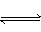 2C(气)达平衡的标志是( )
2C(气)达平衡的标志是( )
A.物质A、B、C的分子个数比为1:3:2
B.单位时间内生成A、C的物质的量之比为1:2
C.单位时间内生成A、B的物质的量之比为1:3
D.反应速率
参考答案:B
本题解析:判断化学反应达到平衡状态的依据是:(1)υ正=υ逆,(2)反应混合物中各组分的百分含量保持不变。本题选项凡假设开始投入2molA和6molB进行反应,当达到平衡状态选项B中A的生成速率是逆反应速率,C的生成速率是正反应速率,两者的比例关系恰恰说明正逆反应速率相等;选项C中A、B的生成速率均表示逆反应速率,没有表达正逆反应速率的关系;选项D没有指明反应速率是正反应速率还是逆反应速率。
本题难度:简单