微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是[???? ]
A.v(H2)=0.1 mol/(L・min)
B.v(N2)=0.1mol/(L・min)
C.v(NH3)=0.15mol/(L・min)
D.v(N2)=0.02mol/(L・s)
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列可逆反应中,正反应是吸热反应的是
A.PCl3(l)+Cl2(g) PCl5(s) 降温,PCl3转化率增大
PCl5(s) 降温,PCl3转化率增大
B.NO2(g)+SO2(g) NO(g)+SO3(g) 降温,SO3的体积分数增加
NO(g)+SO3(g) 降温,SO3的体积分数增加
C.2NO2 (g) 2NO(g)+O2(g) 降温,颜色加深
2NO(g)+O2(g) 降温,颜色加深
D.CS2(l)+2H2O(g) CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
参考答案:CD
本题解析:A、降温,PCl3转化率增大,平衡正向移动,正反应放热;
B、降温,SO3的体积分数增加,平衡正向移动,正反应放热;
C、降温,颜色加深,平衡逆向移动,逆向放热,正向吸热;
D、升温,CO2的平衡浓度增大,平衡正向移动,正向吸热。
本题难度:一般
3、选择题 一定温度下,反应N2(g)+3H 2(g)  2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A.混合气体的总质量不再改变
B.混合气体的 平均相对分子质量不再改变
平均相对分子质量不再改变
C.N2与H2的物质的量之和是NH3物质的 量的2倍
量的2倍
D.单位时间里每增加1molN2,同时增加2mol NH3
参考答案:BD
本题解析:略
本题难度:一般
4、填空题 (10分)已知Cu(OH)2沉淀在一定的条件下可以溶解在氨水中,有关反应的化学方程式为:Cu(OH)2+4NH3・H2O [Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
[Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
(1)操作1:在盛有3 mL 0.1 mol・L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol・L-1 NaOH溶液,结果出现蓝色的悬浊液,有关反应的离子方程式为___________。
(2)操作2:在盛有3 mL 0.1 mol・L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol・L-1氨水,结果也出现蓝色的悬浊液,有关反应的离子方程式为___________。
(3)在上述两种悬浊液中分别加入2 mol・L-1的氨水溶解,请从平衡移动的角度思考哪一种悬浊液更易溶解成为清液?___ _______(填“操作1”或“操作2”);理由是_____________。
(4)请你设计一个简单的实验方案验证上述观点(或理由)的可靠性。实验方案:______。
参考答案:(1)Cu2++2OH-=Cu(OH)2↓
(2)Cu
本题解析:略
本题难度:简单
5、填空题 (12分)在一个2L的密闭容器中,投入反应物,发生反应2SO3(g) 2SO2(g)+O2(g)? ΔH>0,其中SO3的变化如下图所示:
2SO2(g)+O2(g)? ΔH>0,其中SO3的变化如下图所示:
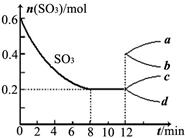
(1)写出该反应的平衡常数表达式并根据8min时到达平衡计算出结果?????????????????。
(2)用O2表示0到8min内该反应的平均速率v=?????????????????。
(3)能说明该反应已达到平衡状态的是???????。
A.v(SO3)=2v(O2) ?????????????????????? B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正????????????????????????????????????D.容器内密度保持不变
(4)在第12min时,容器压缩到1L,则SO3的变化曲线为??????。
A.a???????????? B.b?????????????? C.c????????????? D.d
(5)若保持容积不变在第12min时,加入SO3(g),则平衡向??????反应方向移动(填“正”或“逆”)。SO3的体积分数??????(填“增大”或“减小”)。
参考答案:(1)K= 本题解析:
本题解析:
试题分析:(1)K= ,8分钟时c(SO3)=0.1mol/L,则c(SO2)=0.2mol/L,c(O2)=0.1mol/L,所以K=0.4。
,8分钟时c(SO3)=0.1mol/L,则c(SO2)=0.2mol/L,c(O2)=0.1mol/L,所以K=0.4。
(2)v(O2)=
(3)反应前后压强不等,所以可以用压强不再变化判断反应达平衡,v(SO2)逆=2v(O2)正,正逆反应速率相等,可以判断反应达平衡,因此选BC。
(4)容器压缩的瞬间,SO3物质的量不变,随即平衡逆向移动,SO3的物质的量增大,所以c曲线符合。
(5)若保持容积不变在第12min时,加入SO3(g),相当于对体系加压,平衡正向移动,但SO3的体积分数增大。
点评:本题非常基础,只要掌握影响平衡移动的因素即可。
本题难度:一般