��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��15�֣��ѣ�Ti������Ϊ��������֮��ĵ�������������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ���С������Ⱦ������д���пհף�

��1����ⱥ��ʳ��ˮʱ���÷�Ӧ�����ӷ���ʽ��____________________��
��2����֪����Mg(s)��Cl2(g)=MgCl2(s);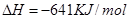
��

�� ____________
____________
��Ӧ��

 ��Ar������������________
��Ar������������________
��3��д���������뽹̿��Cl2�����Ƶ����Ȼ��ѵĻ�ѧ����ʽ______________________
��4���Լ״�������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء���֪��ȼ�ϵ�ص��ܷ�ӦʽΪ��2CH3OH��3O2��4OH��=2CO32����6H2O����ȼ�ϵ�ط�����Ӧʱ��������Һ��PH_____�����������С�����䡱���õ���и����ϵĵ缫��Ӧ��__________.
��5����������ҵ���кϳ�96t�״�����������H2_________t���������������������ʵ��κ���ʧ��
�ο��𰸣���1����2�֣�2Cl����2H2O  ���������
���������
�������������1�����ʳ��ˮ����NaOH��H2��Cl2��
���ø�˹����2��-�ڼ��ɼ������Ӧ��Ϊ��512 KJ/mol������Mg��Ti���н�ǿ��ԭ�ԣ��ڸ����¶���������е�O2��Ӧ�����Է�ӦҪ��Ar�����н��С�
��3�ڼ��Ի����������� O2 + 4e- + 2H2O= 4OH- ���������������ļ�����ǿ�������״�����������Ӧ��CH3OH��6e����8OH��=CO32����6H2O
��5��CO(g)��2H2(g)���� CH3OH(g)
4???????32
X??????
�����Ѷȣ�һ��
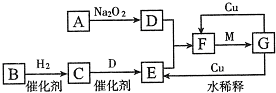
2������� ��ͼ��ʾ�ɶ�����Ԫ����ɵ�һЩ����֮���ת����ϵ��ijЩ��Ӧ��������ȥ�����������ʾ�йص�һ�ַ�Ӧ��������ijЩ�����Ѿ���ȥ��������A��B��D�ڳ����¾�Ϊ��ɫ�̼�����ζ�����壬C��ʹʪ��ĺ�ɫʯ����ֽ���������壬M���������ɫҺ�壮
��1������F�Ļ�ѧʽ��______��
��2������B�ĵ���ʽ��______��
��3��д��C��E�Ļ�ѧ����ʽ��______��
��4��д��G��E�����ӷ���ʽ��______��
�ο��𰸣�C��ʹʪ��ĺ�ɫʯ����ֽ���������壬ӦΪNH3����BΪN2��
���������
�����Ѷȣ���
3������� (12��)��ͼ���ư�����Ԫ������ʾA��B��C��D��E���ֻ����Ԫ�����沿�ִ������ֻ����ﺬ��һ����ͬԪ�أ����ֻ����������ֶ�����Ԫ����ɣ���ÿ�ֻ������������Ԫ����ɣ�A�ǿ�ȼ������Ҫ�ɷ֣�B��E�������������������������(SiH4)���ӵĵ�������ȣ�B���ȶ������н�ǿ�����ԣ��ܷ�������������ԭ��Ӧ��E����Է�������Ϊ32�����л�ԭ�ԣ��ҳ�������������ȼ�ϣ� C�ܷ�����Ӧ��������(��)��������(��)  ������(��)��������(��)��D���������ǽ������ϣ�����������Ԫ�ص�ԭ�Ӹ���֮��Ϊ3��4��������֮��Ϊ3��2.
������(��)��������(��)��D���������ǽ������ϣ�����������Ԫ�ص�ԭ�Ӹ���֮��Ϊ3��4��������֮��Ϊ3��2.

(1) D�Ļ�ѧʽΪ________��
(2)A��B��E�к���һ����ͬ��Ԫ�أ��������ڱ��е�λ��________��
(3)B��E��Ӧ�����ɵ���G�ͳ�����Һ̬������H��д����ѧ����ʽ__________________��
(4)д��C���ϡ�������(��)��������(��)  ������(��)��������(��)���Ļ�ѧ����ʽ________________________________��
������(��)��������(��)���Ļ�ѧ����ʽ________________________________��
�ο��𰸣�(12��)Si3N4��??��һ���ڵڢ�A��??? 2H2O2
�����������
�����Ѷȣ�һ��
4������� ��14�֣�A��J����ѧ��ѧ�г��������ʣ�����֮���ת����ϵ���¿�ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ������

��ش��������⣺
(1)A�Ļ�ѧʽΪ??????????��
(2)H��I��Һ��Ϻ�����Ӧ�����ӷ���ʽ��????????????????��
G��J�Ļ�ѧ����ʽΪ??????????????????????????��
(3)D����ǡ������һ������ϡ������ú��ʵĻ�ѧ�����ʾ������Һ������ԭ��?????????????��
(4) ʵ��֤�������ᷢ��������ԭ��Ӧʱ������Խϡ��Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������C��E�Ͻ���һ�����ĺ�ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���һ��Ũ�ȵ�����������Һ�������������Ƶ����ʵ���������ij��������ʵ�����mol���Ĺ�ϵ����ͼ��ʾ���Իش��������⣺
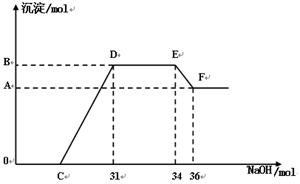
��ͼ��OC��û�г������ɣ��˽η��������ӷ���ʽΪ��_______________________________��
����DE��û�г��������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ��_________________________________��
��B���Ӧ�ij�����Ϊ________________ mol,C���Ӧ�ĺ�����Ϊ___________mol��
�ο��𰸣���1��Al2O3��2�֣�
��2��3AlO2����Al3��
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ����������A����������J��������������D����������C������B��������E������F���Ȼ�������G��������������H��ƫ�����ƣ�I���Ȼ�����
��1���������Ȼ�ѧʽ��Al2O3��
��2��ƫ�����ƺ��Ȼ���ˮ����ٽ�������������������Ӧ�ķ���ʽ��3AlO2����Al3����6H2O=4Al(OH)3�����������������ȶ������ױ�����������������������ʽ��4Fe(OH)2+2H2O+O2�T4Fe(OH)3 ��
��3���������������������Ȼ�
�����Ѷȣ�һ��
5������� �������й����ʵ�ת����ϵͼ(���ֲ�����ʡ��)������AΪ���ʣ�E�ڳ�����ΪҺ�壬D��һ���������壬C����Է�������Ϊ78����ش�������⡣
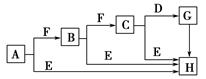
(1)���ж�C�Ľṹ�������ƶ��в���ȷ����?? (����)��
A�������ڿ����л��ɰ�ɫ
B������ǿ������
C�������д������Ӽ���Ǽ��Լ�
D����һ�ּ���������
(2)A��ԭ�ӽṹʾ��ͼΪ____________________��H�ĵ���ʽΪ____________________��E�ĽṹʽΪ____________________��
(3)C��E��Ӧ����H�����ӷ���ʽΪ__________________����Ӧ���������뻹ԭ�������ʵ���֮��Ϊ______��
�ο��𰸣�(1)D��(2) �������������֪��E����Ϊˮ��A��B��C������Ӧ������Ϊ�����������ܷ������������ĵ�����Na��S��C��N2�����ʡ����������������ˮ��Ӧ��ֻ���ơ������ơ��������ƣ��������Ƶ���Է�������Ϊ78����֤��ȷ����AΪ�ơ�FΪ������BΪ�����ƣ�CΪ�������ƣ�DΪ������̼��HΪ�������ơ�(1)A�Na2O2���ÿ��������ձ�ɰ�ɫ��Na2CO3����ȷ��B�Na2O2�У�1�۵����������������л�ԭ�ԣ���ǿ������Ϊ������ȷ��C�Na����O22����������Ӽ���O22���ڲ����ڷǼ��Թ��ۼ�����ȷ��D�Na2O2���ᷴӦ��������
�������������֪��E����Ϊˮ��A��B��C������Ӧ������Ϊ�����������ܷ������������ĵ�����Na��S��C��N2�����ʡ����������������ˮ��Ӧ��ֻ���ơ������ơ��������ƣ��������Ƶ���Է�������Ϊ78����֤��ȷ����AΪ�ơ�FΪ������BΪ�����ƣ�CΪ�������ƣ�DΪ������̼��HΪ�������ơ�(1)A�Na2O2���ÿ��������ձ�ɰ�ɫ��Na2CO3����ȷ��B�Na2O2�У�1�۵����������������л�ԭ�ԣ���ǿ������Ϊ������ȷ��C�Na����O22����������Ӽ���O22���ڲ����ڷǼ��Թ��ۼ�����ȷ��D�Na2O2���ᷴӦ��������
�����Ѷȣ�һ��