微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
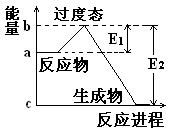
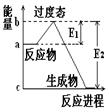
1、填空题 (1) 20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图, 说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的 总能量 (填“大于”、“小于”或“等于”)CO2和NO的总能量。
说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的 总能量 (填“大于”、“小于”或“等于”)CO2和NO的总能量。
(2)在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,在一定条件下发生反应:NO2+CO CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,则:①此段时间内,用CO2表示的平均反应速率为 ②2 min时,容器内气体的总物质的量为_________.
CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,则:①此段时间内,用CO2表示的平均反应速率为 ②2 min时,容器内气体的总物质的量为_________.
参考答案:(1) 放热 大于
本题解析:
试题分析:(1)反应物的总能量高于生成物的总能量,因此该反应时放热反应。所以反应物二氧化氮与一氧化碳的总能量大于产物二氧化碳与一氧化氮的总能量。(2)据题意可算出一氧化氮的速率为0.5除以2再除以2等于0.125 mol/Lmin,化学速率之比等于化学计量数之比,而一氧化碳与一氧化氮的化学计量数比为1;1所以,二氧化碳的速率为0.125mol/Lmin 。NO2+CO CO2+NO,2 min生成了0.5摩尔的一氧化氮,则也会生成0.5摩尔的二氧化碳。同时也会消耗0.5摩尔的一氧化碳和二氧化氮。所以剩余的一氧化碳为2减去0.5等于1.5,剩余的二氧化氮为1.5减去0.5等于1摩尔。所以容器内气体的总物质的量为1.5+1+0.5+0.5等于3.5摩尔
CO2+NO,2 min生成了0.5摩尔的一氧化氮,则也会生成0.5摩尔的二氧化碳。同时也会消耗0.5摩尔的一氧化碳和二氧化氮。所以剩余的一氧化碳为2减去0.5等于1.5,剩余的二氧化氮为1.5减去0.5等于1摩尔。所以容器内气体的总物质的量为1.5+1+0.5+0.5等于3.5摩尔
考点:考查化学反应与能量以及化学反应速率的相关知识
本题难度:一般
2、填空题 (1)P4(白磷,s)+5O2(g)
参考答案:
本题解析:
本题难度:一般
3、选择题 金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。?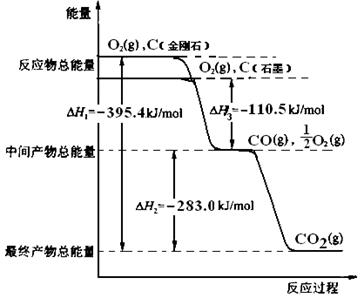
(1)等量金刚石和石墨完全燃烧__________(填“金刚石”或“石墨”)放出热量更多,写出表示石墨燃烧热的热化学方程式___________________________________。
(2)在通常状况下,金刚石和石墨__________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式___________________________。
(3)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量????????????。
参考答案:(1)金刚石(1分) C(石墨s)+O2(g)=CO2(g)
本题解析:(1)从图像上很显然可以看出金刚石能量比石墨高,所以等量金刚石和石墨完全燃烧金刚石放出热量更多,根据燃烧热定义,石墨完全燃烧生成二氧化碳,根据图像反应放出的总热量为110.5+283.0=393.5kJ,所以,表示石墨燃烧热的热化学方程式为C(石墨s)+O2(g)=CO2(g);△H=-393.5kJ/mol(2)因为金刚石能量比石墨高,根据能量越低越稳定,所以在通常状况下石墨更稳定。石墨转化为金刚石要吸收热量,1mol石墨转化为金刚石吸收热量395.4-393.5=1.9kJ,热化学方程式为C(石墨s)
本题难度:简单
4、填空题 化学键的键能是指气态原子间形成1mol化学键时释放的能量。如H(g)+I(g)→H-I(g) △H =+297kJ/mol即H-I键的键能为297kJ.mol-1,也可以理解为破坏1mol H-I键需要吸收297kJ的热量。一个化学反应一般都有旧化学键的破坏和新化学键的形成。下表是一些键能数据(kJ.mol-1):
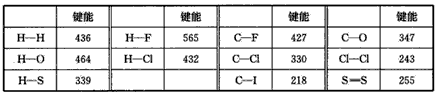
(1)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大)____(填“能”或“不能”)。
②非金属性越强的原子形成的共价键越牢固____(填“能”或“不能”)。
?请从所给数据找出一些规律,并写出其中一条:____;试预测C-Br键的键能范围 ____kJ・mol-1<C-Br键能<___kJ・mol-1。
(2)由热化学方程式H2 (g)+Cl2 (g)=2HCl(g) △H= -185kJ・mol-1,并结合上表数据可推知一个化学反应的反应热(设反应物、生成物均为气态)与反应物和生成物的键能之间的关系是____。 由热化学方程式
2H2 (g)+S2 (s)=2H2S(g) △H= -224. skJ・mol-1和表中数值可计算出1mol S2 (s)气化时将____(填“吸收”或“放出”)____kJ的热量。
参考答案:(1)①不能;②不能;与相同原子结合时,同主族元素形成的共价
本题解析:
本题难度:一般
5、填空题 (1)下列7种固态物质:P4(白磷)、NH4Cl、Ca(OH)2、NaF、CO2、金刚石,回答下列问题(填写化学式或名称):*:%z#zstep.^co&m]
①熔化时不需要破坏化学键的是___??_____,熔化时需要破坏共价键的是_____???___;
②晶体中既有离子键又有共价键的是_____??????????????????___。
③P4(白磷)、SiO2、NaF、CO2四种晶体熔点由高到低的顺序为_____???????????___。
(2)某元素最高正化合价为+6,其最低负价为_____??___。某元素R与氢形成的气态氢化物的化学式为RH3,其最高价氧化物的化学式为____?____。
参考答案:(1)①P4、CO2(1分); SiO2、金刚石(1分) ②
本题解析:
试题分析:离子键是由阴阳离子之间通过静电作用形成的。离子键一般含有金属元素和铵根离子。但是也有特殊例如氯化铝虽然含有金属元素但是他不是属于离子化合物。共价键一般存在于非金属元素之间。晶体的熔点大小由大道小顺序;原子晶体、离子晶体、分子晶体
本题难度:一般