微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于原电池的说法正确的是(???)
A.在正极上发生氧化反应
B.化学性质较活泼的金属为负极
C.在外电路正极电子流出
D.在负极上发生还原反应
参考答案:B
本题解析:依据原电池的工作原理及其电极的选择、电极上所发生的反应和电子流向可得答案。
本题难度:简单
2、选择题 某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
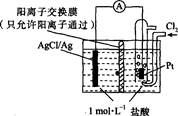
A.正极反应为AgCl+e-
参考答案:
本题解析:
本题难度:一般
3、选择题 关于下列各装置图的叙述中,不正确的是( )
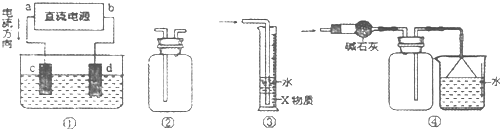
A.装置①中,c为阳极,d为阴极
B.装置②可用于排空气法收集H2、NH3、Cl2、HCl、NO等
C.装置③中X为四氯化碳,可用于吸收氨气或氯化氢
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
参考答案:A.电流由正极流向负极,则a为正极,所以c为阳极,d与负极相
本题解析:
本题难度:一般
4、填空题 (10分)Ⅰ、在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
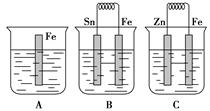
①A中反应的离子方程式为:_______________________________。
②B中Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。
③比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
Ⅱ、如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
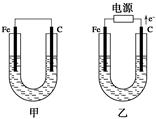
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的________棒。
②乙池中阳极的电极反应式是___________________。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①甲池中碳棒上电极反应式是_____________________,
②乙池电解一段时间后,测知溶液体积为200ml,PH=13,则阴极生成的气体在标准状况下体积是______L。
参考答案:Ⅰ(1)Fe+2H+= Fe2++H2↑ ;(2)
本题解析:
本题难度:一般
5、填空题 (12分)
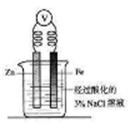
【小题1】下图为牺牲阳极的阴极保护法的实验装置,此装置 中Zn电极上的电极反应为 ;如果将Zn换成Pt,一段时间后,在铁电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,烧杯中的现象是 ,发生的反应的离子方程式是 。

【小题2】CuI是一种不溶于水的白色固体,它可以由反应:2Cu2+ + 4I- = 2CuI↓ + I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。①电解开始不久,阴极产生的实验现象有 ,阴极的电极反应是 。
②阳极区溶液变蓝色,同时伴随的现象还有 ,对阳极区溶液
呈蓝色的正确解释是 。
A.2I- - 2e- = I2;碘遇淀粉变蓝
B.Cu - 2e- = Cu2+;Cu2+显蓝色
C.2Cu + 4I-- 4e- =" 2CuI↓" + I2; 碘遇淀粉变蓝
D.4OH-- 4e- = 2H2O + O2;O2将I-氧化为I2,碘遇淀粉变蓝
参考答案:
【小题1】Zn - 2e-= Zn2+ &
本题解析:(1)锌比铁活泼,作负极失去电子,被氧化,反应式为)Zn - 2e-= Zn2+。如果将Zn换成Pt,则铁是负极,失去电子被氧化生成亚铁离子。原因亚铁离子能和[Fe(CN)6]3-反应生成带有特征蓝色的铁氰化亚铁沉淀,反应式为3Fe2+ + 2[Fe(CN)6]3- =Fe3[Fe(CN)6]2↓。
(2)铜作阳极失去电子被氧化生成铜离子,在阴极上溶液中的氢离子放电生成氢气。由于氢离子是水电离出的,因此随着氢离子的放电,阴极周围水的电离平衡将被破坏 ,使得氢离子浓度降低,OH-浓度增大,溶液显碱性。
(3)由于阳极产生铜离子,因此铜离子可以氧化溶液中的碘离子生成单质碘和碘化亚铜白色沉淀。因为铜离子被消耗,所以溶液显蓝色,不是因为铜离子的原因,而是由于生成的单质碘遇到淀粉而产生的。
本题难度:一般