��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ҵ������������У�SO2�ڽӴ����б�������ΪSO3����֪�÷�ӦΪ���ȷ�Ӧ���ֽ�2 mol SO2��1 mol O2����һ�ܱ�������ַ�Ӧ�ų�����98.3 kJ����ʱ���SO2��ת����Ϊ50%�������Ȼ�ѧ����ʽ��ȷ����
A��2SO3(g)  2SO2(g)��O2(g) ��H����196.6 kJ��mol��1
2SO2(g)��O2(g) ��H����196.6 kJ��mol��1
B��2SO2(g)��O2(g)  SO3(g)��H����98.3 kJ��mol��1
SO3(g)��H����98.3 kJ��mol��1
C��SO2(g)��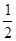 O2(g)
O2(g) SO3(g)��H����98.3 kJ��mol��1
SO3(g)��H����98.3 kJ��mol��1
D��SO2(g)��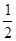 O2(g)
O2(g) SO3(g)��H����196.6 kJ��mol��1
SO3(g)��H����196.6 kJ��mol��1
�ο��𰸣�A
�����������ԭ�ϵ�����SO2��ת����Ϊ50%��֪��1 mol SO2��ȫ��Ӧ�ų�����98.3 kJ�����Ȼ�ѧ����ʽΪSO2(g)��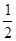 O2(g)
O2(g) �����Ѷȣ���
�����Ѷȣ���
2��ѡ���� ���ݡ�C�����ʯ��=C��ʯī������H= ��1.896kJ��mol��1�������Եó�����ȷ������
A��ʯī�������Ƚ��ʯ��
B��ʯī�ͽ��ʯ����̼��ͬλ��
C�����ʯת��Ϊʯī�������仯
D�����ʯ��ʯī���ȶ�
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3��ѡ���� ��֪���Ͽ�1molN��N��Ҫ����akJ�������Ͽ�1molH��H��Ҫ����bkJ�������Ͽ�1molN��H��Ҫ����ckJ��������ij�ܱ�������ͨ��1molN2��3molH2����һ�������·�����Ӧ��N2(g)+3H2(g) 2NH3(g)�����ȷ�Ӧ����������������ȷ����
2NH3(g)�����ȷ�Ӧ����������������ȷ����
A��N2��H2���е�������һ����NH3���е���������
B��a��b��c���ߵĹ�ϵΪ��a+3b��2c
C�����ܱ�������ͨ��1molN2��3molH2����Ӧ�ų���������Ϊ(6c�Da�D3b)kJ
D���γ�1molN��H��ų�ckJ����
�ο��𰸣�D
���������
���������A��N2(g)+3H2(g) 2NH3(g)���˷�Ӧ�Ƿ��ȷ�Ӧ������������NH3���������ڷ�Ӧ��N2��H2���е�������������B��a��b��c���ߵĹ�ϵΪ��a+3b��2c������C��N2(g)+3H2(g)
2NH3(g)���˷�Ӧ�Ƿ��ȷ�Ӧ������������NH3���������ڷ�Ӧ��N2��H2���е�������������B��a��b��c���ߵĹ�ϵΪ��a+3b��2c������C��N2(g)+3H2(g) �����Ѷȣ�һ��
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ����[???? ]
A���ڻ�ѧ��Ӧ�����У��������ʱ仯��ͬʱ��һ�����������仯
B���¼�����ʱ�ͷŵ����������ھɼ�����ʱ���յ�������ʱ����ӦΪ���ȷ�Ӧ
C����Ӧ��������ʴ��ڷ�Ӧ�������ʱ����Ӧ���ȣ���H>O
D����H�Ĵ�С���Ȼ�ѧ����ʽ�ļ���ϵ����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ���³�ѹ�£��ڴ�����ͬ�����������ݻ���ȵļס�����������ֱ���ж��������Ϳ������ֱַ������������ʵ�飺��N2O4 2NO2?��H�� 0��
2NO2?��H�� 0��

��a�������������ڷ�ˮ�м��ȷ�
��b���ڻ����϶���2 kg������
������������£����������������С�ıȽϣ���ȷ����
A����a����>�ң�b����<��
B����a����>�ң�b����=��
C����a����<�ң�b����>��
D����a����>�ң�b����>��
�ο��𰸣�A
���������
���������
����������÷�Ӧ���������ġ����ȵĿ��淴Ӧ�������������ڷ�ˮ�м��ȣ���ƽ��������Ӧ�����ƶ���������������������ڻ����϶���2 kg�����룬���൱��������ѹǿ��ƽ�����淴Ӧ�����ƶ��������С�ĸ��࣬����ʱ�������С�������������ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ӱ���ۺ���ǿ�����ض�ѧ�����������ͼ��ɵ�������ѵ��������������ѧ���������������ͳ���˼ά���������ѧ����Ӧ��������ѧϰЧ�ʡ�
�����Ѷȣ���