微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 据报道,科学家研制出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是( )

参考答案:B
本题解析:水分解需要吸热,所以产物的总能量大于反应物的总能量,排除A、C选项;加入催化剂可以降低反应的活化能,故选项B正确。
本题难度:简单
2、选择题 下列叙述中正确的是?????????(???)
A.热化学方程式2H2(g)+O2(g)====H2O(l);ΔH="-571.6" kJ・mol-1中ΔH表示H2的燃烧热
B.分子晶体的熔点、沸点随共价键增强而升高
C.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
参考答案:C
本题解析:A中1 mol H2完全燃烧的反应热表示H2的燃烧热。B中分子晶体的熔沸点与分子间作用力有关,与共价键强弱无关。D项如:简单阴离子的核外电子排布应与本周期稀有气体元素原子的核外电子排布相同。
本题难度:一般
3、选择题 已知某反应的△H=-150kJ?mol-1,下列有关该反应的叙述正确的是( )
A.该反应的反应物总能量低于生成物总能量
B.逆反应活化能一定小于150?kJ?mol-1
C.正反应活化能小于150?kJ?mol-1
D.逆反应活化能比正反应活化能大150?kJ?mol-1
参考答案:A、该反应为放热反应,所以反应物总能量大于生成物总能量,故A
本题解析:
本题难度:简单
4、选择题 已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ・mlo-1、-1411.0kJ・mlo-1和-1366.8kJ,则由C2H4(g)和H2O(I)反应生成C2H5OH(I)的△H为
A.-44.2kJ・mol-1
B.+44.2kJ・mlo-1
C.-330kJ・mol-1
D.+330kJ・mlo-1
参考答案:A
本题解析:根据题意可知,①C2H4(g)+3O2(g)=2CO2(g)+2H2O(l)?ΔH= -1411.0kJ/mol,②C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(l)?ΔH= -1366.8kJ/mol。根据盖斯定律可知,①-②即得到C2H4(g)+H2O(I)=C2H5OH(1),所以反应热是-1411.0kJ/mol+1366.8kJ/mol=-44.2kJ/mol,答案选A。
本题难度:简单
5、填空题 已知化学反应N2+3H2 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
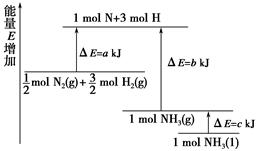
(1)1 mol N和3 mol H生成1 mol NH3(g)是________能量的过程(填“吸收”或“释放”)。
(2)由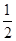 ?mol N2(g)和
?mol N2(g)和 ?mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)________kJ能量。
?mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)________kJ能量。
参考答案:(1)释放 (2)释放 b-a
本题解析:如果反应物具有的总能量大于生成物具有的总能量,整个反应就放出能量,反之就吸收能量。(1)由图像可知1 mol N和3 mol H具有的总能量比1 mol NH3(g)高 b kJ,所以1 mol N和3 mol H生成1 mol NH3(g)是释放能量的过程。(2)由图像可知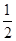 mol N2(g)和
mol N2(g)和![]()
本题难度:一般