微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某研究性学习小组为确定某纯净碱式碳酸镁样品的组成,设计出了下图所示的实验装置(图中A至D的部分)。[已知碱式碳酸镁Mgx(OH)y(CO3)z(x、y、z为正整数)加热能分解生成氧化镁、水和二氧化碳]
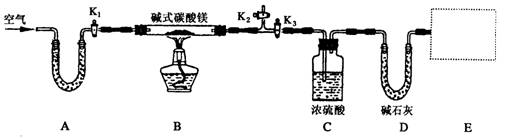
(1)按上图(夹持仪器未画出)组装好实验装置后,应首先进行的操作是__________;A处U形管盛放的药品是__________________,其作用为_______________________。
(2)指导老师在审阅设计方案后指出需要在E处增加一装置,你认为该装置应该是_____________________________.
(3)加热前需要向该装置缓缓鼓入空气数分钟,其目的是___________________;此时对活塞的操作方法是:打开活塞____________________,关闭活塞_________________。
(4)关闭活塞K1、K2,打开K3,加热一段时间后,同学们发现C处洗气瓶中几乎没有气泡冒出,这是由于_________________________。
(5)反应完全后,打开K1,再缓缓鼓入空气数分钟,其目的是_____________________。
(6)实验测得数据如下:碱式碳酸镁样品22.6 g;反应前C装置的质量为87.6 g,反应后质量为89.4 g;反应前D装置的质量为74.7 g,反应后质量为83.5 g。请计算推导该碱式碳酸镁的化学式______________________,该碱式碳酸镁受热分解的化学方程式为____________。
2、简答题 某化学兴趣小组在课外活动中,对某溶液进行了三次检验,每次检验结果如下表所示,请回答下列问题.
| 检验次数 | 溶液中检验出的物质
第一次
KCl、K2SO4、Na2CO3、NH4Cl
第二次
NH4Cl、BaCl2、Na2SO4、K2CO3
第三次
Na2SO4、NH4Cl、K2CO3、NaCl
(1)三次检验结果中第______次检验结果不正确.
(2)检验时,为了证明溶液中存在SO42-、Cl-、CO32-,进行下列实验:(填写下列空白)
| 步骤 | 实验操作 | 预期现象及结论
1
向溶液中滴加______(填化学式)溶液至过量
______
2
______
______
3
过滤,再向滤液中加入______(填化学式)溶液
______
(3)步骤1中溶液滴加过量的目的是______;如何判断步骤2中的溶液已加过量______.
3、选择题 进行化学实验,观测实验现象,通过分析推理得出正确的结论是学习化学的方法之一。对下列实验事实的解释正确的是
A.在KI淀粉溶液中通入Cl2,溶液变蓝,说明氯气能与淀粉发生显色反应
B.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸
C.在某溶液中加入HNO3酸化的BaCl2溶液有白色沉淀产生,说明溶液中含有SO42-
D.将铜片放入浓硫酸中无明显实验现象,说明铜在冷的浓硫酸中发生钝化
4、实验题 (13分)实验室要配制1 mol・L-1的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸 mL
(2)配制时,必须使用的仪器有 (填代号)
①烧杯 ②100 mL量筒 ③20 mL量筒 ④1000 mL容量瓶 ⑤250 mL容量瓶 ⑥托盘天平(带砝码) ⑦玻璃棒还缺少的仪器是 。
(3)配制时,该实验两次用到玻璃棒,其作用分别是 ????? 、 。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”)
①没有洗涤烧杯和玻璃棒。 。
②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。
③容量瓶没有干燥。
④定容时俯视容量瓶瓶颈刻度线????????????????????
5、填空题 某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
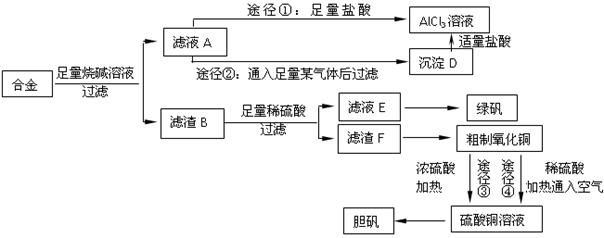
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式????????????????????????????,有人认为合金与烧碱溶液形成了原电池,则作为原电池负极的物质是???????????。
(2)由滤液A制AlCl3溶液的途径有①和②两种,你认为合理的是??????????????????????。上述实验方案多处采用了过滤操作,过滤所用到的玻璃仪器有????????????????????和玻璃棒;其中玻璃棒的作用是?????????????????。
(3)用粗制氧化铜通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是:????????????????????????????、????????????????????????????????????。
(4)通过途径④实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、?????????????????????、冷却结晶、?????、自然干燥。其中“加热通氧气”所起的作用为?????????????????????????????????????????????(用离子方程式表示)。
(5)在测定所得胆矾(CuSO4・xH2O)中结晶水x值的实验过程中:称量操作至少进行????次。若测定结果x值偏高,可能的原因是?????????。
a.加热温度过高?? b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却???????????? d.胆矾来源:91考试网 91ExaM.org晶体部分风化????????????
e.加热时胆矾晶体飞溅出来?????????? f.所用坩埚事先未干燥(潮湿)
|
|