微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 氧化铁和铁粉的混合物19.2 g,恰好溶于150 mL某浓度的稀硫酸,并收集到3.36 L(标准状况下)的气体。向反应后的溶液中滴加硫氰化钾溶液,不显血红色。求:
(1) 原混合物中铁粉的质量。
(2) 稀硫酸的物质的量浓度。
2、实验题 细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”。其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O??2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO?4)3+8H2O????15FeSO4+ 8H2SO4
Cu2S(辉铜矿)+2Fe?2(SO4)2????2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式:????????????????????????????????????????????。
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
物质
| Cu(OH)2
| Fe(OH)2
| Fe(OH)3
|
开始沉淀pH
| 6.0
| 7.5
| 1.4
|
沉淀完全pH
| 13
| 14
| 3.7
实验室有下列试剂可供选择A.H2O2 ???B.CaO? C.CuO?? D.稀H2SO4??E.铁粉;???
实验经过滤后还需设计的实验操作步骤和目的是:
实验步骤
| 实验操作
| 实验操作的目的
| 步骤1
| ?
| ?
| 步骤2
| ?
| ?
| 步骤3]
| ?
| ?
| 步骤4
| 洗涤
| ?
| 步骤5
| ?
| 得到FeSO?4溶液
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数。该实验小组的方法是向m g混合物中加人足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g。已知Cu2O溶于稀硫酸生成Cu和CuSO4。某学生据此计算出该混合物Cu2O的质量分数的计算式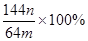 。该学生的计算是否正确:???????????????,请说明理由???????????????????????????????????????????????????????????????。 。该学生的计算是否正确:???????????????,请说明理由???????????????????????????????????????????????????????????????。
3、选择题 下列反应中,改变反应物的用量或浓度,不会改变反应产物种类的是( )
A.碳粉在氧气中燃烧
B.铁在氧气中燃烧
C.CO2通入氢氧化钠溶液
D.铜和硝酸溶液反应
4、选择题 有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的浓度为( )
A.0.5 mol/L
B.3.0 mol/L
C.2.0 mol/L
D.1.0 mol/L
5、选择题 把一定量的铁粉放入含三价铁离子溶液中,反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等,则已反应Fe3+的和未反应的Fe3+物质的量之比是( )
|
|
网站客服QQ: 960335752 - 14613519 - 791315772