微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镁―次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+ H2O + 2e-= Cl-+ 2OH-,关于该电池的叙述正确的是
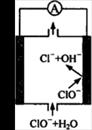
A.该电池中镁为负极,发生还原反应
B.电池工作时,OH-向正极移动
C.电池工作时,正极周围溶液的pH将不断变小
D.该电池的总反应为:Mg + ClO-+ H2O = Mg(OH)2↓+ Cl-
参考答案:D
本题解析:
试题分析:A.该电池中镁为负极,发生氧化反应.Mg-2e-+ 2OH-= Mg(OH)2↓。错误. B.根据同种电荷相互排斥,异种电荷相互吸引的原则,在电池工作时,OH-向正电荷较多的负极移动。错误。C.在电池工作时,由于正极发生反应为:ClO-+ H2O + 2e-= Cl-+ 2OH-,所以正极周围溶液的pH将不断变大。错误。D.根据正极、负极的电极反应式可知该电池的总反应为:Mg + ClO-+ H2O = Mg(OH)2↓+ Cl-。正确。
本题难度:一般
2、选择题 下列有关说法正确的是
A.锌锰干电池中,锌电极是正极
B.电解MgCl2饱和溶液,可制得金属镁
C.锡青铜(铜锡合金)文物在潮湿环境中的腐蚀比干燥环境中快
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
参考答案:C
本题解析:略
本题难度:简单
3、选择题 用锌片、铜片和硝酸银组成的原电池,正极上发生的电极反应是????????(????)
A.2H++2e-=H2↑
B.Zn-2e-=Zn2+
C.2H2O+O2+4e-=4OH-
D.Ag++e-=Ag
参考答案:D
本题解析:锌比铜活泼,锌作负极,铜作正极,溶液中的Ag+放电,方程式为Ag++e-=Ag。答案D。
本题难度:简单
4、选择题
图甲中电极均为石墨电极,下列叙述中正确的是
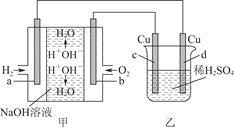
A.电子沿a→d→c→d路径流动
B.b极的电极反应为O2+4e-+4H+=2H2O
C.通电初期乙中的总反应为Cu+H2SO4  CuSO4+H2↑
CuSO4+H2↑
D.反应过程中,甲、乙装置中溶液的pH都逐渐减小
参考答案:C
本题解析:
电子可以沿着导线流动,在电解质溶液中是阴阳离子的移动产生电流,即电子沿a→d、c→b路径流动;电池电解质为NaOH,所以b电极的电极反应为O2+4e-+2H2O=4OH-;反应过程中,甲装置中产生水,所以溶液的pH减小,但是乙装置中由于H+被消耗,所以pH增大。
本题难度:一般
5、选择题 镍镉(Ni
参考答案:
本题解析:
本题难度:一般