ͼ11
?
230���ʵ��������Ӧ��������??????������ĸ�������¶��¹�ҵ�������˲��õĺϳ������n(H2):n(CO) �ı�ֵ��Χ��????????������ĸ����A��1��1.5??????? B��2.5��3??????C��3.5��4.5
��3���Ƽ״�����Ҫ���������������з�Ӧ��ȡ��H2O(g)+CO(g) H2(g)+CO2(g) ��H��0��ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=1���Իش��������⣺
H2(g)+CO2(g) ��H��0��ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=1���Իش��������⣺
�ٸ��¶��£�����ʼʱc(CO)="1" mol��L-1��c(H2O)="2" mol��L-1����Ӧ����һ��ʱ����H2��Ũ��Ϊ0.5 mol��L-1�����ʱ�÷�Ӧv(��)???????v(��)���>������<����=������
���������¶ȣ��÷�Ӧ��Kֵ��???????�����������?????С�����䡱����
��4��ijʵ��С���������ͼ��ʾ�ļ״�ȼ�ϵ��װ�á�
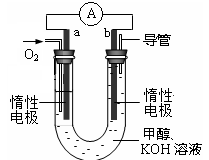
�ٸõ�ع���ʱ��OH����?????���ƶ����a����b������
�ڹ���һ��ʱ������Һ��pH��С���õ�ظ�����ӦʽΪ????????????????????????������ܷ�Ӧ�����ӷ���ʽΪ????????????????????��
�ο��𰸣���1��CH3OH(l)+O2(g)=CO(g)+2H2O(l
�����������1�������˹���ɵ�Ӧ�á����ݷ�Ӧ��CO(g)+1/2O2(g)��CO2(g)�ͷ�Ӧ��2CH3OH(l)+3O2(g)��2CO2(g)+4H2O(l)��֪���ڣ��١�2���õ�2CH3OH(l)+2O2(g)=2CO(g)+4H2O(l)�����Է�Ӧ���ǣ�1453.0kJ/mol��283.0 kJ/mol��2����887 kJ/mol��
��2����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�������¶�Խ�ߣ�ת����Խ�͡���˸���ͼ����ж�����X��ʾ����230�档ͬ������ͼ����жϣ�n(H2):n(CO) �ı�ֵ
�����Ѷȣ�һ��
2��ѡ���� ij������ϡ���ᷴӦ�ų�H2�Ľ�����п���ԭ���ʱ��пΪ��������˽���������
A��Mg
B��Fe
C��Al
D��Cu
�ο��𰸣�B
���������
���������ij������ϡ���ᷴӦ�ų�H2�Ľ�����п���ԭ���ʱ��пΪ��������˽���ֻ����Fe��B��ȷ��
�����Ѷȣ�һ��
3������� ��16�֣�I����һ����NO2��N2O4�Ļ������ͨ�����Ϊ1L�ĺ����ܱ������У�������Ũ����ʱ��仯�Ĺ�ϵ��ͼ1��ʾ��
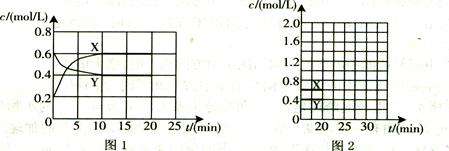
��ش�
��1������ѡ���в���˵���÷�Ӧ�Ѵﵽƽ��״̬���� (��ѡ����ĸ)��
A�������ڻ�������ѹǿ����ʱ��仯���ı�
B�������ڻ��������ܶȲ���ʱ��仯���ı�
C�������ڻ���������ɫ����ʱ��仯���ı�
D�������ڻ�������ƽ����Է�����������ʱ��仯���ı�
��2����Ӧ���е�10 minʱ������������11.38 kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ
��
��3������÷�Ӧ��ƽ�ⳣ��K= ��
��4����Ӧ���е�20 minʱ�����������ڳ���һ����NO2��10min��ﵽ�µ�ƽ�⣬��
ʱ���c(NO2)="0.9" mol��L��
��һ��ƽ��ʱ���������NO2���������Ϊw1���ﵽ��ƽ�����������NO2���������Ϊw2����w1 w2 (�>������=����<��)��
����ͼ2�л���20 min������ʵ�Ũ����ʱ��仯������(�����ϱ�������X����
��Y��)��
II����1����ˮ���Ԫ�ش����dz��ḻ���Ӻ�ˮ����ȡ﮵��о�����DZ����������컯ѧ
��Դ����Ҫԭ�ϡ���LiFePO4�����ij�缫�Ĺ���ԭ������ͼ��ʾ��
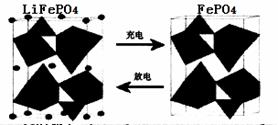
�õ�صĵ����Ϊ�ܴ���Li+�Ĺ�����ϡ��ŵ�ʱ�õ缫�ǵ�ص� ������������������õ缫��ӦʽΪ ��
��2���ô˵�ص�⺬��0.1 mol/L CuSO4��0.1 mol/L NaCl�Ļ����Һ100 mL�������·��ת����0.02 mol e�����ҵ��صĵ缫��Ϊ���Ե缫�����������������ڱ�״���µ������__________L.
�ο��𰸣���.��1��B (2��) <
���������
�����������.��1��A����Ӧǰ������Ļ�ѧ������֮�Ͳ��ȣ���������ѹǿ����ʱ��ı����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���ȷ��B�����������䣬���Ҳ���䣬�ʻ��������ܶȲ���ʱ��仯���ı䲻����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ�����C��NO2Ϊ����ɫ���壬N2O4Ϊ��ɫ���壬�ʻ���������ɫ����ʱ��仯���ı����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���ȷ��D�����������䣬�����ʵ����ڱ䣬�ʷ�Ӧ�����ƽ�����������ٸı����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���ȷ��
��2����ͼ1��֪����Ӧ��ΪN2O4��������ΪNO2����Ӧ���е�10minʱ��N2O4�����ʵ����仯Ϊ0.2mol/L��1L=0.2mol������������11.38kJ���ʷ�Ӧ1molN2O4����������11.38��5=56.9kJ���ʸ÷�Ӧ�Ȼ�ѧ ����ʽΪ��N2O4��g��?2NO2��g������H=+56.9kJ?mol?1��
��3��k= c2(NO2)/ c(N2O4) =0.62��0.4=0.9��
��4���ٺ��ݣ�����һ����NO2���൱������ѹǿ��ƽ�������ƶ�����ƽ�����������NO2�����������С����W1��W2��
��30minʱ��c��NO2��=0.9mol/L��k=0.92 ��c(N2O4) =0.9��c��N2O4��=0.9mol/L��20min-30min��N2O4��Ũ��������0.9-0.4=0.5mol/L����NO2��Ũ�ȼ�����1mol/L����20minʱ��c��NO2��=1+0.9=1.9mol/L���ɻ���20 min������ʵ�Ũ����ʱ��仯�����ߡ�
��1���ŵ�ʱ����װ����ԭ��أ�FeԪ�ػ��ϼ���+3�۱�Ϊ+2�ۣ��õ��ӷ�����ԭ��Ӧ�����Ըõ缫���������缫��ӦʽΪFePO4+e-+Li+=LiFePO4��
��2������õ�����⺬��0.01mol CuSO4��0.01molNaCl�Ļ����Һ100mL����·��ת����0.02mol e-��
������2Cl- -2e- =Cl2����
0.01mol 0.01mol 0.005mol
4OH--4e-=2H2O+O2����
0.01mol 0.01mol 0.0025mol�������������ɵ������ڱ�״���µ����=��0.005mol+0.0025mol����22.4L/mol=0.168L��
���㣺���⿼��ͼ��ķ������滭����ѧƽ��״̬����ѧƽ�ⳣ�����Ȼ�ѧ����ʽ��ԭ���ԭ����Ӧ�á�
�����Ѷȣ�����
4������� ��13�֣��ɷ�Ǧ��PbS���Ʊ�Pb��PbO2�ķ������£�
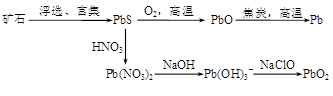
PbO�뽹̿����ʱ���ܻᷢ�����·�Ӧ��
PbO(s)��C(s)��Pb(s)��CO(g)???? ��H����108.5 kJ��mol��1????? ��
PbO(s)��CO(g)��Pb(s)��CO2(g)?? ��H����64 kJ��mol��1??????? ��
��1����֪Pb��O2��Ӧ���Ȼ�ѧ����ʽΪ��2Pb(s)��O2(g)��2PbO(s)? ��H����438 kJ��mol��1
��C��ȫȼ�յ��Ȼ�ѧ����ʽΪ?????��
��2������߷�Ӧ����PbOת���ʵĴ�ʩ��?????������ĸ����
a�������¶�??????? b������ѹǿ??????? c�����뽹̿??????? d���������
��3���Ʊ������л����SO2��NO��CO���ж����壬�ɽ����ǰ�һ�����������һ�������·�Ӧ�õ�S��N2��CO2����SO2��NO�������Ϊ1��2���÷�Ӧ�Ļ�ѧ����ʽΪ???????��
��4��ˮ��Һ��Ǧ�Ĵ�����̬�ж��֣�����̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ��
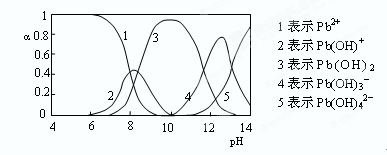
pH��6.5ʱ��Pb2��ˮ������ӷ���ʽΪ?????������NaClO�Ʊ�PbO2֮ǰ������NaOH������ҺpH��12.5��������?????��
�ο��𰸣���1��C(s)��O2(g)��CO2(g)?��H
�����������1�����ݸ�˹���ɿ�֪���٣��ڣ��ۼ��õ�C(s)��O2(g)��CO2(g) �����Է�Ӧ�Ȧ�H����108.5 kJ��mol��1�D64 kJ��mol��1�D438 kJ��mol��1����393.5 kJ��mol��1��
��2������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ���ת���ʽ��ͣ���Ӧǰ��������䣬�ı�ѹǿƽ�ⲻ�ƶ�����������Ӱ��ƽ��״̬�����뽹̿��������CO2������CO2Ũ�ȣ�ƽ��������Ӧ�����ƶ���ת��������ѡc��
��3�����ݻ��ϼ۵ı仯��֪��SO2��CO�ǻ�ԭ����NO������
�����Ѷȣ�һ��
5��ѡ���� ����ͼ��ʾʵ��װ�õ� K �պϣ������ж���ȷ����
A��Cu �缫�Ϸ�����ԭ��Ӧ
B�������� Zn��a��b��Cu ·������
C��Ƭ�̺�׳���c(SO42-)����
D��Ƭ�̺�ɹ۲쵽��ֽb����ɫ
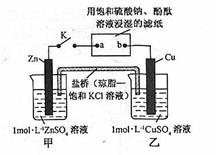
�ο��𰸣�A
���������K�պ�ʱ��Zn��������ͭƬ����������ԭ��أ�ʹ��aΪ������bΪ��������ⱥ����������Һ��A���ȷ��B��ڵ����е��Ӳ�������������Һ�У�����C��׳������������û�зŵ磬����Ũ�Ȳ��䡣����D�bΪ������OH-�ŵ磬ʹ��b������Һ�����ԣ�����ʹ��ֽ��죬����
�����㶨λ�����⿼����ԭ��غ͵���ԭ����
�����Ѷȣ�һ��