微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铜锌原电池工作时,下列叙述正确的是(???)

A、正极反应为:Zn―2e-=Zn2+
B、B、在外电路中,电子从铜片流向锌片
C、电池反应为:Zn+Cu2+=Zn2+ +Cu
D、盐桥中的K+移向ZnSO4溶液
参考答案:C
本题解析:
试题分析:A:锌极发生氧化反应,是负极;B:锌极失去电子被氧化,铜极得到电子被还原,在外电路电子是从锌极流向铜极;D:盐桥中的溶液是电解质溶液,由于锌极失去电子成为Zn2+
进入溶液,使ZnSO4溶液带正电,所以盐桥中的Cl-会移向ZnSO4溶液,使溶液保持电中性,氧化还原反应得以继续进行,故D错。
点评:本题考查原电池的工作原理,难度不大,注意基础知识的积累。
本题难度:一般
2、选择题 下列关于铜、锌和稀硫酸构成的原电池说法正确的是
A.锌是正极,铜是负极
B.电子经导线有锌流向铜
C.电流沿导线有锌流向铜
D.H+在溶液中向锌片移动
参考答案:B
本题解析:本题考查铜锌原电池的原理
由铜锌和稀硫酸组成的原电池,正极是铜,负极是锌,所以A错;
正极发生还原反应,电极反应是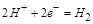 ,则溶液中
,则溶液中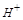 本题难度:一般
本题难度:一般
3、选择题 某新型铝-空气燃料电池,以铝合金为负极,在正极通入空气,若以NaCl溶液或NaOH溶液为电解质溶液,放电时正极反应都为O2+2H2O+4e-=4OH-。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解质溶液,两个电池总反应相同。
B.若以NaOH溶液为电解质溶液,电池负极反应为:Al+4OH--3e-=[Al(OH)4]-
C.电池工作时,电子通过外电路从正极流向负极
D.若以NaOH溶液为电解质溶液,电池在工作过程中电解质溶液的pH保持不变
参考答案:B
本题解析:略
本题难度:一般
4、填空题 (1)铜板上铁铆钉处容易生锈,称为______腐蚀,被腐蚀的金属是______;原电池的正极电极反应式是______.
(2)如图所示的铜-锌原电池中,理论上应观察到的现象是:铜片上:______,此时原电池的负极电极反应式是______.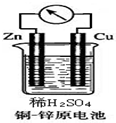
参考答案:(1)铜板上铁铆钉处容易生锈,是因为金属铁、铜、潮湿的空气形
本题解析:
本题难度:一般
5、选择题 如图装置中,在U形管底部盛有 ,分别在U形管两端小心倒入饱和食盐水和饱和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述错误的是
,分别在U形管两端小心倒入饱和食盐水和饱和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述错误的是
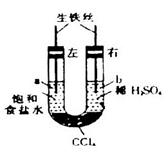
A.铁丝在两处的腐蚀速率: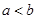
B.a、b两处相同的电极反应式为
C.一段时间后,a处液面高于b处液面
D.生铁丝中的碳在a、b两处分别作原电池的负极和正极
参考答案:D
本题解析:
试题分析:生铁和氯化钠溶液、稀硫酸溶液都能构成原电池,左边试管中,生铁发生吸氧腐蚀,右边试管中,生铁发生析氢腐蚀。A、生铁发生析氢腐蚀的速率比吸氧腐蚀的速率大,正确;B、a处负极上铁失电子,正极上氧气得电子,b处负极上铁失电子,正极上氢离子得电子,所以a、b两处相同的电极反应式为Fe-2e-=Fe2+,正确;C、a处发生吸氧腐蚀,b处发生析氢腐蚀,一段时间后,a处气体压强减小,b处气体压强增大,导致溶液从b处向a处移动,所以a处液面高于b处液面,正确;D、生铁中的碳在a、b两处都作正极,错误。
本题难度:一般