微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
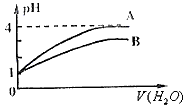
1、选择题 常温下pH=1的两种一元酸溶液A和B,分别加水1000倍稀释,其pH与所加水的体积变化如下图所示,则下列结论中正确的是
 [???? ]
[???? ]
A.A酸比B酸的电离程度小
B.B酸比A酸容易电离
C.B是弱酸,A是强酸
D.pH=1时,B酸的物质的量浓度比A酸大
参考答案:CD
本题解析:
本题难度:一般
2、简答题 某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa
50mL量筒内气体读数 | 反应时间
A瓶
B瓶
|
40mL0.1mol/L
醋酸溶液 | 40mL0.1mol/L
盐酸溶液
5mL
t(a1)=155s
t(b1)=7s
10mL
t(a2)=310s
t(b2)=16s
15mL
t(a3)=465s
t(b3)=30s
20mL
t(a4)=565s
t(b4)=64s
…
…
…
44.8mL
t(an)=865s
t(bn)=464s
(4)在实验数据中:①t(a1)远远大于t(b1)的原因为:______;
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.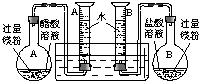
参考答案:(1)在装置中,A、B两个量筒口用胶塞密封,这样反应产生的H
本题解析:
本题难度:一般
3、选择题 在醋酸与氢氧化钠溶液的反应过程中,溶液中的相关离子浓度呈现出下列排列顺序:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。满足该条件的反应是(??? )
A.0.01mol・L-1的CH3COOH与pH=12的NaOH溶液等体积混合
B.0.2 mol・L-1的CH3COOH溶液与0.1 mol・L-1的NaOH溶液等体积混合
C.CH3COOH溶液与NaOH溶液混合后所得溶液的pH=7
D.0.1 mol・L-1的CH3COOH溶液与等物质的量浓度、等体积的NaOH溶液混合
参考答案:B
本题解析:略
本题难度:简单
4、选择题 在20mL0.1mol/L 的醋酸溶液中,能使溶液的pH减小,而且使醋酸的电离平衡向逆方向移动,可加入的试剂是
A.20mL水
B.浓盐酸
C.冰醋酸
D.NaOH溶液
参考答案:B
本题解析:
试题分析:醋酸电离方程式为:CH3COOH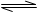 CH3COO-+H+,若使溶液PH降低,且平衡像逆反应方向移动。A选项错误,加水后PH增大,稀释溶液平衡向正反应方向移动。B选项正确。加入浓盐酸后 CH3COO-+H+,若使溶液PH降低,且平衡像逆反应方向移动。A选项错误,加水后PH增大,稀释溶液平衡向正反应方向移动。B选项正确。加入浓盐酸后
PH降低,H+浓度增大,平衡向逆反应方向移动。C选项,加入冰醋酸,PH减小,但平衡向正反应方
向移动。
本题难度:一般
5、填空题 H2O2、CH3COOH是生活中常见的物质,在化学研究中应用广泛。
(1)某小组拟在Fe3+的催化下,探究H2O2分解速率影响的某一因素。限选试剂与仪器:30% H2O2、0.1mol?L-1Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
将表中所给的混合溶液分别加入到2个同容积的锥形瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
锥形瓶编号
| 30% H2O2/mL
| 0.1mol?L-1Fe2(SO4)3/mL
| 蒸馏水/mL
| 反应温度/℃
| 1
| 10
| 1
| 0
| 30
| 2
| Vx
| 1
| 5
| 30
表中Vx= mL,实验目的是 。
(2)醋酸和盐酸是化学实验中常见的二种一元酸,某小组设计下列实验证明它们的电离程度。
实验一:室温下,测出0.1mol?L-1醋酸和盐酸pH值分别为3、1。提示:pH=-lgc(H+)
结论一:醋酸在水溶液中电离 (填“完全”、 “不完全”)。该温度下醋酸的电离度为 ;写出醋酸的电离方程式
实验二:现取等体积、浓度均为1mol?L-1醋酸和盐酸分别加入经砂纸打磨过的表面积相同的镁条。观察放出氢气速率的快慢。
结论二:其它条件相同时,同浓度同体积的一元酸与金属反应时,反应 (填“快”或“慢”)的为弱电解质
参考答案:(1)5,探究H2O2的浓度对分解速率影响
(2)不完
本题解析:
试题分析:据题意可知表1主要探讨H2O2的浓度对分解速率影响,因此加的双氧水的体积为5ml.醋酸属于弱酸,不能完全电离。而电离度(α)= (已电离弱电解质分子数/原弱电解质分子数)*100%,由此可知该温度下醋酸的电离度为1%。取等体积、浓度均为1mol?L-1醋酸和盐酸,弱电解质电离出来的氢离子浓度比盐酸的小,因此与金属反应的反应速率比较慢。
考点:主要考查影响化学反应速率因素以及弱电解质电离的相关知识点。
本题难度:困难
|
|