��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ձ��м������ᣬ���ձ��м�����ᣬ������Һ�������pH ����ȡ��������ձ���ͬʱ�����������ȵ�п������Ӧ������õ�����������������˵������ȷ���� [???? ]
A�����ձ��з���п�����������ձ��з���п������С
B�����ձ��е������
C�����ձ��вμӷ�Ӧ��п����
D����Ӧ��ʼ�����ձ��е�c(H+)ʼ�ձȼ��ձ��е�c(H+)С
2������� ij��Ԫ��H2B�ĵ��뷽��ʽ�ǣ�H2B=H++HB-��HB-?B2-+H+���ش��������⣺
��1��Na2B��Һ��______�ԣ������ǣ������ӷ���ʽʾ��______��
��2��NaHB��Һ��______�ԣ������ǣ������ӷ���ʽ��ʾ��______��
��3����0.1mol?L-1NaHB��Һ��pH=2����0.1mol?L-1H2B��Һ�������ӵ����ʵ���Ũ�ȿ���______���������=��0.11mol?L-1��
��4��0.1mol?L-1NaHB��Һ�и�����Ũ���ɴ�С��˳����______��
3��ѡ���� ��0.05mol NaOH����ֱ��������100mLҺ���У���Һ�ĵ����Ի����������
A������ˮ
B��0.5mol��L-1������
C��0.5mol��L-1�Ĵ���
D��0.5mol��L-1�İ�ˮ
4������� ������Ȼ�糣��������ˮ����������Ca3(PO4)2����ʽ���ڡ����ĵ��ʺͻ��������Ź㷺��Ӧ�á�
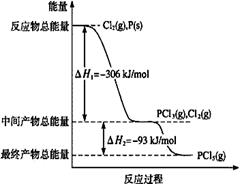
��1������P(s)��Cl2(g)������Ӧ����PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ��ͼ�еġ�H��ʾ����1mol���� �����ݣ���
��ش����⣺
��PCl5�ֽ��PCl3��Cl2���Ȼ�ѧ����ʽ�� ��
��P��Cl2��������Ӧ����1 mol PCl5�ġ�H3�� ��
��2��PCl5�ֽ��PCl3��Cl2�ķ�Ӧ�ǿ��淴Ӧ��T��ʱ����2.0 L�����ܱ������г���1.0 mol PCl5������250 s�ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t / s
| 0
| 50
| 150
| 250
| 350
|
n(PCl3) / mol
| 0
| 0��16
| 0��19
| 0��20
| 0��20
�ٷ�Ӧ��50��150s �ڵ�ƽ������v(PCl3)�� ��
���Լ�����¶��·�Ӧ��ƽ�ⳣ����д��������̣�����2λ��Ч���֣�
��3��NaH2PO4��Na2HPO4��Na3PO4��ͨ��H3PO4��NaOH��Һ��Ӧ��ã��������ֵķֲ�����(ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ���)��pH �Ĺ�ϵ��ͼ��ʾ��

��Ϊ��ýϴ���Na2HPO4��pHӦ������ ��pH��6ʱ����Һ����Ҫ��������Ũ�ȴ�С��ϵΪ�� ��
��Na2HPO4��Һ�ʼ��ԣ�����������CaCl2��Һ����Һ�����ԣ���Һ�����Ե�ԭ���ǣ�������ƽ��Ƕȷ����� ��
5������� һ���ǿ�����ȡ�����ᣬ���Ǹ��ֽⷴӦ�Ĺ���֮һ����֪�ڳ����²��Ũ�Ⱦ�Ϊ0.1mol/L������6����Һ��pH��
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa
pH
8.1
8.8
11.6
10.3
11.1
11.3
��1���������������Ϣ�ж����з�Ӧ���ܷ�������______�����ţ���
A��CH3COOH+NaCN�TCH3COONa+HCN
B��CO2+H2O+2NaClO�TNa2CO3+2HClO
C��2HCN+Na2CO3-��2NaCN+CO2+H2O
D��Na2CO3+C6H5OH-��NaHCO3+C6H5ONa
E��CO2+H2O+C6H5ONa-��NaHCO3+C6H5OH
����֪HA��H2B���������ᣬ�������¹�ϵ��H2B��������+2A-=B2-+2HA����A-��B2-��HB-���������ӽ��H+������˳��Ϊ______��
��2��һЩ���ֽⷴӦ�ķ�������ѭ�������ɣ����б仯�����ڸ��ֽⷴӦ��
�ٽ�ʯ�����봿����Һ��Ͽ��Ƶÿ�������Һ������̼�������Һ�м��뱥��ʳ��ˮ�ɻ��С�մ����??������KCl��NaNO3�Ļ����Һ����������NaCl���壮����������Ӧ���ܽ�����ֽⷴӦ��������һ����Ϊ______��
��3��������ij������ܽ���ˮ�к���Һ�е�c��H+��=10-9mol��L-1����õ���ʿ�����______������ţ���
A��?CuSO4?????B��?HCl???C��?Na2S?????D��NaOH???E��K2SO4
��4�������£���pH=3������a?L�ֱ�������������Һ��ϣ������Һ�������ԣ�
��Ũ��Ϊ1.0��l0-3mol��L-1�İ�ˮb?L��
��c��OH?-��=1.0��10-3mol��L-l�İ�ˮc?L��
��c��OH-��=1.0��10-3mol?L-1������������Һd?L��
��a��b��c��d֮���ɴ�С�Ĺ�ϵ�ǣ�______��
��5��һ���¶��£������������ʵ���Ũ�ȵ�����������Һ����NaOH����CH3COOH����CH3COONa�ֱ�ӵ���ˮ��pH�仯��С����______�����ţ���һ���¶��£���������ˮ�зֱ��������ʵ�����CH3COONa��NaCN������Һ�������ӵ������ʵ����ֱ�Ϊn1��n2����n1��n2�Ĺ�ϵΪn1______n2�����������������=������
��6����֪����ʱKsp��AgCl��=1.8��10-10mol2��L-2����50mL?0.018mo1��L-l��AgNO3��Һ�м�����ͬ���0.020mol��L-1�����ᣬ��c��Ag+��=______����ʱ���û����Һ��pH=______��
|
|