微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,用0.1000mol・L-1NaOH溶液滴定20.00mL 0.1000mol・L-1CH3COOH溶液,滴定曲线如右图。下列说法正确的是
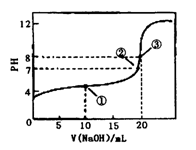
A.点①所示溶液中:[CH3COO-]+[OH-]=[CH3COOH] +[H+]
B.点②所示溶液中:[Na+]=[CH3COOH]+[CH3COO-]
C.点③所示溶液中:[Na+]>[OH-]>[CH3COO-]>[H+]
D.滴定过程中可能出现:[CH3COOH]>[CH3COO-]>
[H+]>[Na+」>[OH-]
参考答案:D
本题解析:A 错误,应遵循电荷守恒,[CH3COO-]+[OH-]=[Na+]+[H+]
B 错误,点②所示溶液PH=7,显中性,[Na+]=[CH3COO-]
C 错误,点③所示溶液中:[Na+]>[CH3COO-]>[OH-]>[H+]
D 正确。在CH3COOH溶液中开始滴入很少量的NaOH溶液时出现此种情况。
本题难度:一般
2、选择题 某酸HX稀溶液和某碱YOH稀溶液的物质的量浓度相等,两溶液混合后,溶液的pH大于7,下表中判断合理的是
编号
| HX
| YOH
| 溶液的体积关系
|
①
| 强酸
| 强碱
| V(HX)=V(YOH)
|
②
| 强酸
| 强碱
| V(HX)<V(YOH)
|
③[
| 强酸
| 弱碱
| V(HX)=V(YOH)
|
④
| 弱酸
| 强碱
| V(HX)=V(YOH)
A.①③ B.②③ C.①④ D.②④
参考答案:D
本题解析:分析:①一元强酸和一元强碱等浓度、等体积混合后,溶液pH=7;
②等浓度的一元强酸和一元强碱混合,如碱体积大,碱过量,溶液呈碱性;
③等浓度、等体积的一元强酸和一元弱碱混合,反应后溶液呈酸性;
④等浓度、等体积的一元弱酸和一元强碱混合,反应后溶液呈碱性.
解答:解:①一元强酸和一元强碱等浓度、等体积混合后,n(H+)=n(OH-),完全反应后,溶液pH=7,故①错误;
②等浓度的一元强酸和一元强碱混合,如碱体积大,碱过量,n(H+)<n(OH-),溶液呈碱性,pH>7,故②正确;
③等浓度、等体积的一元强酸和一元弱碱混合,反应后生成强酸弱碱盐,溶液水解呈酸性,pH<7,故③错误;
④等浓度、等体积的一元弱酸和一元强碱混合,反应后强碱弱酸盐,溶液水解成碱性,pH>7,故④正确.
故选D.
本题难度:简单
3、选择题 能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( ) A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化碳气体
D.向水中加食盐晶体
参考答案:C
本题解析:
本题难度:一般
4、填空题 (14分)在温度t℃下,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入pH=b的NaHSO4,测得混合溶液的部分pH如下表所示:
序号
| 氢氧化钡的体积/mL
| 硫酸氢钠的体积/mL
| 溶液的pH
| ①
| 33.00
| 0.00
| 8
| ②
| 33.00
| x
| 7
| ③
| 33.00
| 33.00
| 6
(1)依据题意判断,t℃___________25℃(填“大于”、“小于”或“等于”),该温度下水的离子积常数Kw = ___________。
(2)b=____________,x =" ______mL" 。
(3)反应③的离子方程式为____________________________
(4)将此温度下的Ba(OH)2溶液取出1mL,加水稀释至1L,则稀释后溶液中
c(Ba2+)
参考答案:
本题解析:
本题难度:一般
5、填空题 (1)①写出NaHSO4在水溶液中的电离方程式______.
②CO2通入足量氢氧化钠溶液反应的离子反应方程式______.
③OH-+H+=H2O改写为化学方程式______.
Cu2++Fe=Fe2++Cu改写为化学方程式______.
(2)①同温同压下,某瓶充满氧气时质量为116g,充满二氧化碳时,质量为122g,充满气体A时质量为114g,A的摩尔质量为______.
②现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol.若阿伏加德罗常数用NA表示,则该气体所含原子总数为______个.
(3)下列实验操作中不正确的是______(多选).
A.用分液的方法分离水和汽油的混合物B.用过滤的方法分离饱和食盐水与沙子的混合物
C.蒸馏时,应使温度计水银球插入液面以下D.蒸发结晶时应将溶液蒸干后再停止加热
E.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出.
参考答案:(1)NaHSO4在水溶液中完全电离出三种离子,即NaHSO
本题解析:
本题难度:一般
|
|
网站客服QQ: 960335752 - 14613519 - 791315772