微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关防止或减少酸雨的措施中不可行的是
A.对含SO2、NO2的废气处理后再排空
B.人工收集大气雷电产生的氮的氧化物
C.对燃煤及燃煤烟气进行脱硫
D.推广天然气、甲醇等作为汽车的燃料
参考答案:B
本题解析:分析:A.二氧化硫和二氧化氮都是有毒气体,会污染大气,不能直接排空;
B.人工收集大气雷电产生的氮的氧化物不现实,且容易遭雷击;
C.煤中含有硫元素,煤燃烧后的烟气中含有二氧化硫,二氧化硫有毒且是形成酸雨的主要成分之一;
D.甲醇和天然气燃烧后生成二氧化碳和水,对环境无污染.
解答:A.二氧化氮和二氧化氮有毒,会污染环境,所以对含有SO2、NO2的废气处理后再排空,故A正确;
B.大气雷电产生的氮氧化物被豆科植物直接吸收,人工不可以收集,故B错误;
C.煤中含有硫元素,对燃煤及燃煤烟气进行脱硫,防止生成二氧化硫或防止生成的二氧化硫污染空气,故C正确;
D.天然气、甲醇燃烧后生成二氧化碳和水,对环境无污染,所以推广天然气、甲醇等作为汽车的燃料,故D正确;
故选B.
点评:本题考查了有关酸雨的问题,明确形成酸雨的成分、来源是解本题的关键,难度不大.
本题难度:困难
2、填空题 (4分)将20g Ba(OH)2?8H2O固体与10g NH4Cl晶体在烧杯中混合,不断搅拌,实验现象为:?????????????????????????????????????????????????????????????,
该反应的化学方程式:?????????????????????????????????????????????????
参考答案:容器外壁变冷(1分),固体变成糊状(1分),有刺激性气体放出
本题解析:考查化学反应中的能量变化。氢氧化钡晶体和铵盐的反应是吸热反应,导致周围环境的温度降低。强碱和铵盐反应会放出氨气,氨气是有刺激性气味的。
本题难度:一般
3、选择题 在测定中和热的实验中,下列说法正确的是
A.使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5mol・L-1NaOH溶液分别与0.5 mol・L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同
D.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
参考答案:A
本题解析:A正确,搅拌可加快反应速率,减小热量损耗;B错,实验中温度计水银球不能与小烧杯底部接触;C错,盐酸为强酸而醋酸为弱酸,弱酸电离要吸收能量,两者所测中和热数值不同;D错,在测定中和热实验中没有使用到天平;
本题难度:一般
4、选择题 已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ・mlo-1、-1411.0kJ・mlo-1和-1366.8kJ,则由C2H4(g)和H2O(I)反应生成C2H5OH(I)的△H为
A.-44.2kJ・mol-1
B.+44.2kJ・mlo-1
C.-330kJ・mol-1
D.+330kJ・mlo-1
参考答案:A
本题解析:根据题意可知,①C2H4(g)+3O2(g)=2CO2(g)+2H2O(l)?ΔH= -1411.0kJ/mol,②C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(l)?ΔH= -1366.8kJ/mol。根据盖斯定律可知,①-②即得到C2H4(g)+H2O(I)=C2H5OH(1),所以反应热是-1411.0kJ/mol+1366.8kJ/mol=-44.2kJ/mol,答案选A。
本题难度:简单
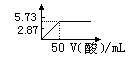
5、选择题 已知H+(aq)+OH―(aq)= H2O(l);ΔH= -57.kJ/mol,向50mL2mol/L的NaOH溶液中加入1mol/L的某种酸,测得加入酸的体积与反应放出的热量关系如右图所示(不考虑热量损失),则该酸可能是????????(???)
A.盐酸
B.醋酸
C.草酸(HOOC-COOH)
D.硫酸
参考答案:C
本题解析:因50mL的酸与NaOH恰好反应完,故它应是二元酸,又生成0.1mol水时放出的热量小于5.73kJ,故酸为弱酸。
本题难度:简单