微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,
下列说法正确的是(??)
A.起始时盐酸和醋酸溶液PH相同
B.V(NaOH)=10.00 mL 时,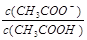 <1
<1
C.pH=7时,两种酸所用NaOH溶液体积不相等,醋酸用的体积多
D.V(NaOH)="20" .00 mL 时,c(Cl?)>c(CH3COO―)
2、选择题 某温度下向20mL 0.1 mol・L-1 CH3COOH溶液中逐滴加入0.1 mol・L-1 NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图(忽略温度变化)。下列说法中正确的是(??)
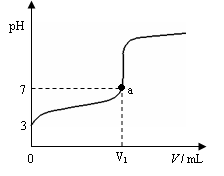
A.该温度下醋酸的电离平衡常数约为1×10-5mol・L-1
B.图中V1 > 20mL,且a点对应的溶液中:
c (Na+)+ c (H+) = c (OH-)+ c (CH3COO-)
C.图中V1 < 20mL,且a点对应的溶液中:
c (CH3COOH) + c (CH3COO-)<c (Na+)
D.当加入Na OH溶液的体积为20mL时,溶液中:
c (CH3COOH) + c (H+) > c (OH-)
3、填空题 现有室温下浓度均为1×10-3mol/L的几种溶液①盐酸、②硫酸、③醋酸、④氯化铵、⑤氨水、⑥NaOH溶液,回答下列问题:
(1)PH均等于3的溶液①、②、③、④中水电离产生的c(H+)的比值是?????????
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③???⑥(填“>”、“<”或“=”),溶液中的离子浓度由大到小的顺序为?????????????????????????????????????????
(3) 将等体积的①、⑤混合,则溶液的PH?????7(填“>”、“<”或“=”),用离子方程式说明其原因??????????????????????????????????????????????????
(4)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为????????????,最终产生H2总量的关系为?????????????????
(5)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的PH大小关系为①??????③(填“>”、“<”或“=”)
(6)若将等体积的⑤、⑥溶液加热至相同温度后,溶液的PH⑤????⑥(填“>”、“<”或“=”)
4、选择题 下列热化学方程式中的反应热下画线处表示燃烧热的是[???? ]
A.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) △H= -akJ/mol
B.CH3CH2OH(l)+1/2O2(g)=CH3CHO(l)+H2O(l) △H=-bkJ/mol
C.CO(g)+1/2O2(g)=CO2(g) △H=-ckJ/mol
D.NH3(g)+5/4O2(g)=NO(g)+6/4H2O(g) △H=-dkJ/mol
5、选择题 C、CO、CH4、C2H5OH是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、283.0kJ、890.3kJ、1?366.8kJ。相同质量的这4种燃料,完全燃烧时放出热量最多的是 [???? ]
A、C?????????????
B、CO????????????
C、CH4?????????????
D、C2H5OH