微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度(℃)
| 10
| 20
| 30
| 加热煮沸后冷却到50℃
|
pH
| 8.3
| 8.4
| 8.5
| 8.8
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:___________________________
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确。试剂X是 。
A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 (填“甲”或“乙”)判断正确。
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH―浓度分别为amol /L和bmol /L,则a与b的比值= 。
2、选择题 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
①将水加热煮沸??? ②向水中投入一小块金属钠??
③向水中通CO2???? ④向水中通NH3??? ⑤向水中加入明矾晶体??????
⑥向水中加入NaHCO3固体??? ⑦向水中加NaHSO4固体
A.①③⑥⑦
B.①③⑤⑥
C.⑤⑦
D.⑤
3、选择题 室温下,在pH=12的某溶液中,由水电离的c(OH-)为( )
①1.0×10-7mol.L-1 ②1.0×10-6mol.L-1 ③1.0×10-2mol.L-1 ④1.0×10-12mol.L-1
A.③
B.③④
C.①③
D.④
4、选择题 对水的电离平衡不产生影响的粒子是( )
A.Fe3+
B.Cl-
C.HCl
D.CH3COO-
5、选择题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液浓度和混合所得溶液的pH如下表所示
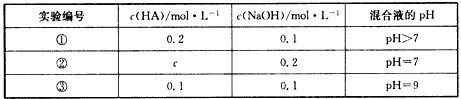
下列说法中,不正确的是 [???? ]
A.由实验①可知,HA为弱酸
B.实验①所得混合溶液:c(Na+)>c(A-)>c(OH-)>c(H+)
C.实验②所得混合溶液:c(Na+)=c(A-)
D.实验③所得混合溶液中由水电离出的OH-的浓度为1×10-9 mol/L
|