微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应
后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色。

①出现这种现象的原因,除了因“铁块”中可能混有没反应完的
磁性氧化铁外,还有一种可能原因是 。
② 若要证明反应所得“铁块”中含有金属铝,可用 (填化学式)溶液,所发生反应的离子方程式为 。
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H+ + 4I-+ O2 = 2I2 + 2H2O。该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率。已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深。
实验小组拟用0.8 mol・L-1 KI溶液、0.1 mol・L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A―C三组实验,部分实验数据如下表:
编号
| 温度/℃
| H2SO4体积/mL
| KI溶液体积/mL
| H2O体积/mL
| 淀粉溶液
/ mL
| 出现蓝色时间 /s
|
A
| 39
| 10
| 5
| 5
| 1
| 5
|
B
| TB
| 10
| 5
| 5
| 1
| 没出现蓝色
|
C
| 5
| 10
| 5
| 5
| 1
| 39
|
D
|
|
|
|
|
| t
①为确保A组实验在39℃下进行,应采用的控温操作方法是 。
②A―C三组实验时,都加入了5mL水,其目的是 。
③B组实验中“没出现蓝色”,原因是 。
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标。
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结
论 。
2、选择题 用NH3制取硝酸的第一步反应为:4NH3+5O2 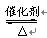 4NO+6H2O。对该反应的有关说法错误的是 4NO+6H2O。对该反应的有关说法错误的是
A.该反应是可逆反应
B.反应中NH3能全部转化为NO
C.催化剂能加快该反应的速率
D.升高温度能加快该反应的速率
3、填空题 (8分)为了研究MnO2与双氧水(H2O2)的反应速率,某学生加少许的MnO2粉末于 50 mL密度为1.1g?cm-3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示。请依图回答下列问题:
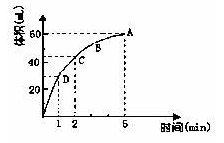
(1)实验时放出气体的总体积为 ___ ;
(2)放出一半气体所需要的时间为 ___ ;
(3)ABCD四点化学反应速率的由快到慢顺序为 ____ _______ ;
(4)在5min后,收集到的气体体积不再增加,原因是 。
4、选择题 在其他条件具备时,若一反应较难进行,则其主要原因可能是( )
①参加反应的分子的能量普遍较低
②参加反应的分子的能量普遍较高
③单位时间内反应物活化分子有效碰撞次数较少
④单位时间内反应物活化分子有效碰撞次数较多
⑤反应物分子中活化分子百分数较小
⑥反应物分子中活化分子百分数较大.
A.①③⑤
B.②④⑥
C.①④⑥
D.②③⑤
5、选择题 25℃、101kPa?下:
①2Na(s)+1/2O2(g)=Na2O(s)???△H1=-414KJ/mol ?????????????????????
②2Na(s)+O2(g)=Na2O2(s)?????△H2=-511KJ/mol
下列说法正确的是 [???? ]
A、①和②产物的阴阳离子个数比不相等???
B、①和②生成等物质的量的产物,转移电子数不同
C、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D、25℃、101kPa?下,Na2O2(s)+2?Na(s)=?2Na2O(s)??△H=-317kJ/mol
|