微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以下实验目的能达到的是(? )
A.测Zn的相对原子质量可以通过测Zn的质量以及这些Zn和过量的稀硫酸反应时放出H2的体积
B.测Na2CO3、NaHCO3混合物中Na2CO3的质量分数可以通过测样品的质量及样品和过量Ba(OH)2溶液反应的沉淀的质量
C.测中和热时,可以用稀氨水代替NaOH溶液
D.将淀粉溶液滴入某混合液中,检验是否含有碘化钾
参考答案:B
本题解析:A项:气体的体积与温度、压强有关,必须记录或换算为标准状况;C项:NH3・H2O为弱电解质,电离时会吸热。B项由m(混合物)和m(沉淀)两个条件列方程组求解;D项淀粉只能检验碘分子存在,不能检验碘离子存在,D错误。
本题难度:一般
2、实验题 某化学兴趣小组利用如图所示装置(部分夹持仪器已省略) 进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题。
|
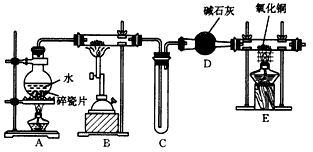
(1)E中的现象是__________________。
(2)A、B两个装置中应先点燃____处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是_________。
参考答案:(1)黑色固体变为红色,硬质玻璃管右端管壁有液滴生成
本题解析:
本题难度:一般
3、填空题 有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、NaCl??CaCl2等物质组成,为鉴别它们做了如下实验:①将固体溶于水,搅拌,得无色溶液.②向此溶液中滴入BaCl2溶液有白色沉淀生成.③过滤,然后在此白色沉淀中加入足量的稀盐酸,沉淀最后全部消失.则固体混合物中肯定有______???肯定没有______可能含有______.
参考答案:①取固体混合物样品溶于水搅拌后得到无色溶液,由于硫酸铜溶液为
本题解析:
本题难度:一般
4、实验题 某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
(1)用下列实验装置制取干燥纯净的氯气??
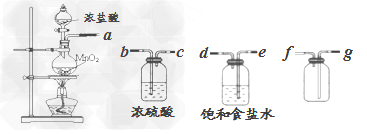
①制备并收集得到干燥纯净的氯气,上述各装置按气流从左到右方向连接顺序为______________(填仪器接口的字母编号)
②该实验还存在不足之处,应如何改进?_________________________
(2)某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
①提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:____________;假设③:_____________。
②设计实验方案:取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。

由此得出结论:假设_____________成立(填序号①②③)。
(3)为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Fe(OH)3溶解度小于Mg(OH)2溶解度
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
(4)a溶液常作印刷电路铜板的腐蚀剂,得到含有Cu2+等的废液,有人提出可以利用如图的装置从得到的废液中提炼金属铜。该过程中甲池负极的电极反应式是____________,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为?_______________(假设气体全部逸出)。

参考答案:(1)①aedbcgf? ;②在C后接NaOH溶液尾气处理装
本题解析:
本题难度:一般
5、实验题 电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。
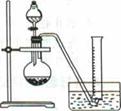
实验原理:CaC2 +2H2O==Ca(OH)2+C2H2 ↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①称取样品1.2g;
②把1.2g样品放入气密性良好的气体发生装置,如图所示;
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平;
④作为反应器的烧瓶中有24mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽、?????????、?????????、???????????。
(2)若实验前有1000mL、500 mL、250 mL的量筒备用,则应选用???????????mL的量筒。
(3)生成气体体积是???????????mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是????。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,反应的化学方程式为□KMnO4+□C2H2+□H2SO4――□K2SO4+□MnSO4+□CO2+□?????。若该实验生成的C2H2完全被KMnO4溶液氧化,至少需0.1 mol・L-1的KMnO4溶液???????????mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为??。
参考答案:(1)圆底烧瓶;分液漏斗;量筒
(2)500
(
本题解析:
试题分析:(1)从装置图中可以看出,玻璃仪器还有圆底烧瓶、分液漏斗和量筒。
(2)量筒中收集到气体360mL,因此应选择500mL的量筒。
(3)因为反应容器中的液体会使反应器中原有的空气进入量筒,因此收集到气体的体积为360mL-24mL=336mL。量筒读数时应注意使量筒内外液面相平,视线与量筒内液面的最低处相切。
(4)反应中,Mn的化合价由+7降至+2,降低5价,C的化合价由-1升至+4,升高5价,根据氧化还原反应得失电子守恒及原子守恒,可配平方程式。根据方程式可知:2KMnO4~C2H2,乙炔的物质的量为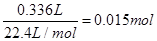 ,则需要高锰酸钾溶液的体积为
,则需要高锰酸钾溶液的体积为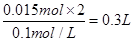 ,即300mL。
,即300mL。
(5)电石的纯度为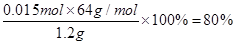 。
。
本题难度:一般